去勢抵抗性前立腺がんの放射線治療薬が国内承認
投稿者:羊毛 投稿日:2025/10/15(水) 11:01:45 No.88
[返信]
メルマガ登録している「がんプラス」で、次のような記事がありました。
-----
【週刊】がんプラスPickupニュース(2025年9月29日)
前立腺がんの標的放射性リガンド療法「プルヴィクト」が国内承認
https://cancer.qlife.jp/news/article32479.html
ノバルティス、PSMA陽性転移性去勢抵抗性前立腺がんの治療における日本初の標的放射性リガンド療法として「プルヴィクト®静注」の承認を取得
https://www.novartis.com/jp-ja/news/media-releases/prkk20250919
-----
転移していて去勢抵抗性になった前立腺がんで、放射性同位体(ルテチウム-177)を含んだ治療薬を注射する治療(PSMA標的治療)がありますが、その治療を受けるためには海外に行かなくてはいけない、というものです。
西郷輝彦さんが2021年にオーストラリアで受けた治療と思います。
「国内承認」の意味が分かりませんでしたが、AIによると次の通り。
保険適用はまだ先のようですが、国内承認が取れたので、自費でも国内で治療をする病院が現れてくれるといいですね。
-----
「薬事承認」は、医薬品や医療機器が有効性・安全性について国の基準を満たしているかを審査し、厚生労働大臣が認めることです。一方、「保険適用」は、薬事承認された医薬品が健康保険の対象となるかを厚生労働省が決定することです。薬事承認がなければ保険適用はできませんが、薬事承認されても保険適用までには審査期間がさらに必要になります。
-----
-----
【週刊】がんプラスPickupニュース(2025年9月29日)
前立腺がんの標的放射性リガンド療法「プルヴィクト」が国内承認
https://cancer.qlife.jp/news/article32479.html
ノバルティス、PSMA陽性転移性去勢抵抗性前立腺がんの治療における日本初の標的放射性リガンド療法として「プルヴィクト®静注」の承認を取得
https://www.novartis.com/jp-ja/news/media-releases/prkk20250919
-----
転移していて去勢抵抗性になった前立腺がんで、放射性同位体(ルテチウム-177)を含んだ治療薬を注射する治療(PSMA標的治療)がありますが、その治療を受けるためには海外に行かなくてはいけない、というものです。
西郷輝彦さんが2021年にオーストラリアで受けた治療と思います。
「国内承認」の意味が分かりませんでしたが、AIによると次の通り。
保険適用はまだ先のようですが、国内承認が取れたので、自費でも国内で治療をする病院が現れてくれるといいですね。
-----
「薬事承認」は、医薬品や医療機器が有効性・安全性について国の基準を満たしているかを審査し、厚生労働大臣が認めることです。一方、「保険適用」は、薬事承認された医薬品が健康保険の対象となるかを厚生労働省が決定することです。薬事承認がなければ保険適用はできませんが、薬事承認されても保険適用までには審査期間がさらに必要になります。
-----
Re: 去勢抵抗性前立腺がんの放射線治療薬が国内承認
投稿者:羊毛 投稿日:2025/10/15(水) 11:27:29 No.89
国内で治験した病院も調べてみました。
PSMA陽性mCRPCを有する患者を対象とした治験薬(PSMA標的化放射性リガンド)の国内第2 相試験
https://novartis.ct-match.com/clinical-trial/%E5%89%8D%E7%AB%8B%E8%85%BA%E3%81%8C%E3%82%93/
北海道大学病院、福島県立医科大学附属病院、国立がん研究センター東病院、横浜市立大学附属病院、金沢大学附属病院、京都大学医学部附属病院、神戸市立医療センター中央市民病院、千葉県がんセンター
PSMA陽性mCRPCを有する患者を対象とした治験薬(PSMA標的化放射性リガンド)の国内第2 相試験
https://novartis.ct-match.com/clinical-trial/%E5%89%8D%E7%AB%8B%E8%85%BA%E3%81%8C%E3%82%93/
北海道大学病院、福島県立医科大学附属病院、国立がん研究センター東病院、横浜市立大学附属病院、金沢大学附属病院、京都大学医学部附属病院、神戸市立医療センター中央市民病院、千葉県がんセンター
私の参加した寡分割照射の臨床試験の結果がプレプリント版であるが発表された。
筆頭著者は浜松医科大学の中村和正氏。
https://www.researchsquare.com/article/rs-3217050/v1
臨床試験の目的はこう書かれている。
前立腺癌に対して画像誘導技術を用いた強度変調放射線治療による寡分割照射法70 Gy/28回(1回2.5 Gy)が有効かつ安全であるかを探索的に検討する。
以下のように報告されている。
リスク分類別患者数
低リスク 20 人
中間リスク 80 人
高リスク 34 人
合計 134人
高リスクは「高リスク因子(T3a, 20< PSA =<30, G=8,9)の一つのみを有する」
さらに「中リスクまたは高リスクの前立腺がん患者には、4~8か月の術前補助ホルモン療法が必須」
5年全生存率:94.5%
5年PSA非再発率:96.0%
5年臨床的無再発生存率:99.2%
5年PSA非再発率
低リスク:94.1%
中間リスク:97.4%
高リスク:93.9%
5年後のグレード2の消化器系および泌尿生殖器系の晩期毒性発現率は、それぞれ5.3%および5.3%
グレード3以上の急性毒性および晩期毒性は認められなかった。
...(続きを読む)
日本人の前立腺癌患者を対象としたこの試験で、中等度寡分割IMRTの安全性と有効性が確認された。
私が患者として参加した臨床試験の論文で私の属性、中間リスクでかなり良好な結果が報告されたのは素直にうれしい。高リスクもそれなりのPSA再発率が報告されたのはやはり高リスク因子は一つのみという制約があったからだろう。
論文の終わりに書かれている次の文は臨床試験に参加したものとして意義深いものだ。
「私たちの試験は、アジア諸国で前立腺がんに対する中等度寡分割放射線治療が普及するためのマイルストーンになると考えている」
筆頭著者は浜松医科大学の中村和正氏。
https://www.researchsquare.com/article/rs-3217050/v1
臨床試験の目的はこう書かれている。
前立腺癌に対して画像誘導技術を用いた強度変調放射線治療による寡分割照射法70 Gy/28回(1回2.5 Gy)が有効かつ安全であるかを探索的に検討する。
以下のように報告されている。
リスク分類別患者数
低リスク 20 人
中間リスク 80 人
高リスク 34 人
合計 134人
高リスクは「高リスク因子(T3a, 20< PSA =<30, G=8,9)の一つのみを有する」
さらに「中リスクまたは高リスクの前立腺がん患者には、4~8か月の術前補助ホルモン療法が必須」
5年全生存率:94.5%
5年PSA非再発率:96.0%
5年臨床的無再発生存率:99.2%
5年PSA非再発率
低リスク:94.1%
中間リスク:97.4%
高リスク:93.9%
5年後のグレード2の消化器系および泌尿生殖器系の晩期毒性発現率は、それぞれ5.3%および5.3%
グレード3以上の急性毒性および晩期毒性は認められなかった。
...(続きを読む)
日本人の前立腺癌患者を対象としたこの試験で、中等度寡分割IMRTの安全性と有効性が確認された。
私が患者として参加した臨床試験の論文で私の属性、中間リスクでかなり良好な結果が報告されたのは素直にうれしい。高リスクもそれなりのPSA再発率が報告されたのはやはり高リスク因子は一つのみという制約があったからだろう。
論文の終わりに書かれている次の文は臨床試験に参加したものとして意義深いものだ。
「私たちの試験は、アジア諸国で前立腺がんに対する中等度寡分割放射線治療が普及するためのマイルストーンになると考えている」
Re: 前立腺癌に対するIMRT/IGRT併用寡分割照射法の第II相臨床試験
投稿者:羊毛 投稿日:2023/09/20(水) 12:12:43 No.87
眞さんの投稿、変なところで「(続きを読む)」が表示されてますね~。
時間のある時に調査・対応します。m(__)m
時間のある時に調査・対応します。m(__)m
ADT後のテストステロンの回復について
投稿者:ぽんた 投稿日:2021/04/28(土) 10:27:31 No.73
[返信]
前立腺癌患者におけるADT(ホルモン療法)後のテストステロン(男性ホルモン)の回復
(Testosterone recovery profiles after cessation of androgen deprivation therapy for prostate cancer) J Sex Med 16: 872-879, 2019
アメリカのSexual & Reproductive Medicine Program, Urology Service, Memorial Sloan Kettering Cancer Center, NYというところからの論文
重粒子線治療後1年半行う予定のADTがそろそろ終わりに近づきましたので、いろいろ悩まされていますホルモン療法からの回復はどのようなものかと情報を得たくてこの論文を読んで見ました。
まずテストステロンの血中の値についていくつかの数値を規定しています。
① 非去勢レベル: >50ng/dl
② 正常レベル : >300ng/dl
③ 基礎値 : これはADT開始前の各自のテストステロン値
自分の場合は600ng/dlでした。
<方法、結果>
307人の患者(平均年齢65歳)について検討。ADTの平均期間は17か月、ADT後の経過観察の平均は31か月。基礎値の平均は379ng/dl, ADT後24か月経過後の平均は321ng/dl。24か月経過後、8%の患者が去勢レベルにとどまる。76%が正常値を回復、51%が基礎値に復帰。テストステロンの正常値への回復と有意に相関する要因は低い基礎値(400ng/dl以下)、ADTの期間(6か月以上)。年齢が65歳以上、6か月以上のADTはテストステロン回復が緩やか。
<感想>
年齢、ADT期間の平均がほぼ自分と同じ対象で、テストステロンは2年待てば、それなりに回復するのだと少し安心しました。ただこれは血中のテストステロン値の回復のみの話で、ADTに伴ういろいろな副作用の経過がどうなるのかといったことはまた別問題だと思いますので、次回はADT終了後の諸症状の経過について検討した論文を読んで見たいと思います。
(Testosterone recovery profiles after cessation of androgen deprivation therapy for prostate cancer) J Sex Med 16: 872-879, 2019
アメリカのSexual & Reproductive Medicine Program, Urology Service, Memorial Sloan Kettering Cancer Center, NYというところからの論文
重粒子線治療後1年半行う予定のADTがそろそろ終わりに近づきましたので、いろいろ悩まされていますホルモン療法からの回復はどのようなものかと情報を得たくてこの論文を読んで見ました。
まずテストステロンの血中の値についていくつかの数値を規定しています。
① 非去勢レベル: >50ng/dl
② 正常レベル : >300ng/dl
③ 基礎値 : これはADT開始前の各自のテストステロン値
自分の場合は600ng/dlでした。
<方法、結果>
307人の患者(平均年齢65歳)について検討。ADTの平均期間は17か月、ADT後の経過観察の平均は31か月。基礎値の平均は379ng/dl, ADT後24か月経過後の平均は321ng/dl。24か月経過後、8%の患者が去勢レベルにとどまる。76%が正常値を回復、51%が基礎値に復帰。テストステロンの正常値への回復と有意に相関する要因は低い基礎値(400ng/dl以下)、ADTの期間(6か月以上)。年齢が65歳以上、6か月以上のADTはテストステロン回復が緩やか。
<感想>
年齢、ADT期間の平均がほぼ自分と同じ対象で、テストステロンは2年待てば、それなりに回復するのだと少し安心しました。ただこれは血中のテストステロン値の回復のみの話で、ADTに伴ういろいろな副作用の経過がどうなるのかといったことはまた別問題だと思いますので、次回はADT終了後の諸症状の経過について検討した論文を読んで見たいと思います。
ホルモン療法に伴う手指関節症状
投稿者:ぽんた 投稿日:2021/01/15(金) 19:46:10 No.72
[返信]
Prevalence of hand joint symptoms in Androgen Deprivation Therapy among Japanese Patients with prostate cancer Urological Science 31:15-20, 2020.Shogo Inoue et al
邦題:日本人前立腺癌患者におけるホルモン療法に伴う手関節症状について
広島大学泌尿器科からの論文です。自分自身がホルモン療法によるばね指および関節症状に悩んでいるもので、なかなか論文が見つからず、やっと探し出した文献です。
ホルモン療法を受けた患者150人に関して、受けていない患者129人を対照として、手指の症状(関節痛、手指のしびれ、手指の筋力低下)の出現がどの程度差があるかを調べたものです。手指関節症状はホルモン治療を受けた患者の16.7%に見られ、受けていない患者より有意に多かったというのが結果の骨子です。著者も考察で述べていますが、患者側では、ばね指を含む関節症状はよく知られた副作用であるにも関わらず、医療者側ではそれほど問題となる症状との認識に乏しいようです。メカニズムの詳細は不明ですが、女性の乳がん治療で、エストロゲンを減らす治療(aromatase inhibitorと呼ばれる薬剤だそうですが)で、やはり手指の関節症状、こわばり感が出現し、こちらはよく知られているそうです。男女共に性ホルモンというのは筋・骨格・関節といった運動機能と密接に関連しているのは間違いがないようです。
邦題:日本人前立腺癌患者におけるホルモン療法に伴う手関節症状について
広島大学泌尿器科からの論文です。自分自身がホルモン療法によるばね指および関節症状に悩んでいるもので、なかなか論文が見つからず、やっと探し出した文献です。
ホルモン療法を受けた患者150人に関して、受けていない患者129人を対照として、手指の症状(関節痛、手指のしびれ、手指の筋力低下)の出現がどの程度差があるかを調べたものです。手指関節症状はホルモン治療を受けた患者の16.7%に見られ、受けていない患者より有意に多かったというのが結果の骨子です。著者も考察で述べていますが、患者側では、ばね指を含む関節症状はよく知られた副作用であるにも関わらず、医療者側ではそれほど問題となる症状との認識に乏しいようです。メカニズムの詳細は不明ですが、女性の乳がん治療で、エストロゲンを減らす治療(aromatase inhibitorと呼ばれる薬剤だそうですが)で、やはり手指の関節症状、こわばり感が出現し、こちらはよく知られているそうです。男女共に性ホルモンというのは筋・骨格・関節といった運動機能と密接に関連しているのは間違いがないようです。
重粒子線+ADT後のPSAの変化
投稿者:ぽんた 投稿日:2021/01/09(土) 21:08:22 No.71
[返信]
Prostate-specific antigen dynamics after neoadjuvant androgen-deprivation therapy
and carbon ion radiotherapy for prostate cancer
邦訳:ホルモン療法(ADT)を併用した重粒子線治療後のPSA変化
Yosuke Takakusagi 他
PLoS ONE 15(11): e0241636. https://doi.org/10.1371/journal.pone.0241636
Published: November 6, 2020
PloS Oneというネット雑誌掲載の論文、神奈川がんセンター放射線科から。
照射前、ADTを併用し、重粒子線治療を行った85例の中間リスク前立腺癌患者を対象とし治療後のPSAの経過を経時的に経過を追った論文
自分が重粒子線治療を約8か月前に終了し、あと4か月ほどでADTを終了しようかというところなので、今後のPSAの経過について検討した論文を読んでみました。
治療時期は2015年から2017年、ADTは重粒子線終了と同時に止めている。
Bounce(バウンス)の定義はnadir(最低値)から0.4ng/ml以上のPSAの上昇
PSA failure(生化学的再発)の定義は通常通り、nadirから2ng/ml以上の上昇
平均follow up期間は30か月(20~48)
PSA bounceは39例(45.9%)に見られた。
PSA failreは8例(9.4%)に見られたとのこと。
PSA bounceが見られた症例と相関のあった要因は若年であることのみとのことです。
興味深いのはPSA failureの判定基準を満たした8例のうち、7例が治療の追加なくPSA値がその後低下していることです。これらは本当に再発なのか。そもそも放射線治療単独の場合とADTを併用した場合との再発の基準を、ともにnadir+2ng/mlに設定するのはおかしいのではないかと思います。ADTを併用すると正常細胞のPSA産生も機能的に抑えるわけで、ADTの終了後のPSAの戻りが大きいのは当然と考えられます。したがってそもそもADT+放射線治療のPSA再発の基準は、nadir+2ng/mlよりも高い値に設定すべきなのではないでしょうか。
and carbon ion radiotherapy for prostate cancer
邦訳:ホルモン療法(ADT)を併用した重粒子線治療後のPSA変化
Yosuke Takakusagi 他
PLoS ONE 15(11): e0241636. https://doi.org/10.1371/journal.pone.0241636
Published: November 6, 2020
PloS Oneというネット雑誌掲載の論文、神奈川がんセンター放射線科から。
照射前、ADTを併用し、重粒子線治療を行った85例の中間リスク前立腺癌患者を対象とし治療後のPSAの経過を経時的に経過を追った論文
自分が重粒子線治療を約8か月前に終了し、あと4か月ほどでADTを終了しようかというところなので、今後のPSAの経過について検討した論文を読んでみました。
治療時期は2015年から2017年、ADTは重粒子線終了と同時に止めている。
Bounce(バウンス)の定義はnadir(最低値)から0.4ng/ml以上のPSAの上昇
PSA failure(生化学的再発)の定義は通常通り、nadirから2ng/ml以上の上昇
平均follow up期間は30か月(20~48)
PSA bounceは39例(45.9%)に見られた。
PSA failreは8例(9.4%)に見られたとのこと。
PSA bounceが見られた症例と相関のあった要因は若年であることのみとのことです。
興味深いのはPSA failureの判定基準を満たした8例のうち、7例が治療の追加なくPSA値がその後低下していることです。これらは本当に再発なのか。そもそも放射線治療単独の場合とADTを併用した場合との再発の基準を、ともにnadir+2ng/mlに設定するのはおかしいのではないかと思います。ADTを併用すると正常細胞のPSA産生も機能的に抑えるわけで、ADTの終了後のPSAの戻りが大きいのは当然と考えられます。したがってそもそもADT+放射線治療のPSA再発の基準は、nadir+2ng/mlよりも高い値に設定すべきなのではないでしょうか。
High-risk Prostate Cancer Treated With Dose-escalated RT: An Analysis of Hormonal Therapy Use and Duration, and Prognostic Implications of PSA Nadir ?0.2 to Select Men for Short-term Hormonal Therapy
Am J Clin Oncol. 2017 Aug;40(4):348-352. doi: 10.1097/COC.0000000000000161.
邦題:高線量放射線治療を施行した高リスク前立腺癌患者における内分泌療法についての検討
<コメント>60歳台、PSA7.0 GS4+4=8 T2a 転移なし
昨年12月からADT,今年6月に重粒子線治療を受けています。ADTによる筋力低下、全身倦怠、手指のこわばり、関節痛など(重篤なものではありません、旅行にも行けています)に悩んでおり、出来ればADTは1年で終了にしたいと思っております。重粒子線後PSAは0.008まで低下しています。ADTの中止は、満更冒険でもないように思い、理論武装に励んでおります。
この論文はレバノンからのものであるのが少々気になりますが、私の選択を基礎づけてくれるものでしたので、投稿させていただきます。
<抄録>
目的:通常高リスク前立腺患者に対して放射線治療を施行する場合には、内分泌療法(男性ホルモン除去療法:ADT)が併用される。ADTは副作用を伴い、ADLを低下させる。したがって可能であれば短期間での終了が望ましい。短いADT期間で良好な予後が期待できる患者群を選択しうる要因について検討した。
方法:1988年から2009年、458人の転移を認めない高リスク前立腺患者を対象。平均照射線量は76.4Gy ADT無し(105人) 短期ADT(12か月以下、194人) 長期ADT(12か月以上 160人)。遠隔転移無生存(freedom from distant metastasis:FFDM)、非前立腺癌死生存(cause-specific survival:CSS)について検討。平均経過観察は71か月
結果:7年FFDMは83%、CSSは91%。多変量解析によれば、nadir PSA(経過中のPSAの最低値)が0.2以下及びGleason score(GS)がFFDM、CSSと統計的有意に関連。ADTを施行した期間は予後と関連無し。PSA nadir <=0.2ng/mlでは良好な転帰。GS9はPSA nadirが0.2以下であっても予後は不良。この群は長期間ADTを行うことでCSSが改善
結論:高リスク群であっても対象を選べば、長期のADTは不要かも知れない。GS9以上ではなく、かつPSA nadir<=0.2を達成できれば、短期間のADTで良好な予後を期待できる可能性がある。
Am J Clin Oncol. 2017 Aug;40(4):348-352. doi: 10.1097/COC.0000000000000161.
邦題:高線量放射線治療を施行した高リスク前立腺癌患者における内分泌療法についての検討
<コメント>60歳台、PSA7.0 GS4+4=8 T2a 転移なし
昨年12月からADT,今年6月に重粒子線治療を受けています。ADTによる筋力低下、全身倦怠、手指のこわばり、関節痛など(重篤なものではありません、旅行にも行けています)に悩んでおり、出来ればADTは1年で終了にしたいと思っております。重粒子線後PSAは0.008まで低下しています。ADTの中止は、満更冒険でもないように思い、理論武装に励んでおります。
この論文はレバノンからのものであるのが少々気になりますが、私の選択を基礎づけてくれるものでしたので、投稿させていただきます。
<抄録>
目的:通常高リスク前立腺患者に対して放射線治療を施行する場合には、内分泌療法(男性ホルモン除去療法:ADT)が併用される。ADTは副作用を伴い、ADLを低下させる。したがって可能であれば短期間での終了が望ましい。短いADT期間で良好な予後が期待できる患者群を選択しうる要因について検討した。
方法:1988年から2009年、458人の転移を認めない高リスク前立腺患者を対象。平均照射線量は76.4Gy ADT無し(105人) 短期ADT(12か月以下、194人) 長期ADT(12か月以上 160人)。遠隔転移無生存(freedom from distant metastasis:FFDM)、非前立腺癌死生存(cause-specific survival:CSS)について検討。平均経過観察は71か月
結果:7年FFDMは83%、CSSは91%。多変量解析によれば、nadir PSA(経過中のPSAの最低値)が0.2以下及びGleason score(GS)がFFDM、CSSと統計的有意に関連。ADTを施行した期間は予後と関連無し。PSA nadir <=0.2ng/mlでは良好な転帰。GS9はPSA nadirが0.2以下であっても予後は不良。この群は長期間ADTを行うことでCSSが改善
結論:高リスク群であっても対象を選べば、長期のADTは不要かも知れない。GS9以上ではなく、かつPSA nadir<=0.2を達成できれば、短期間のADTで良好な予後を期待できる可能性がある。
内分泌療法の期間
投稿者:ぽんた 投稿日:2020/08/20(木) 09:06:53 No.68
Duration of Androgen Deprivation Therapy in High-risk Prostate Cancer: A Randomized Phase III Trial
Eur Urol. 2018 Oct;74(4):432-441. doi: 10.1016/j.eururo.2018.06.018.
高リスク前立腺癌患者における内分泌療法(ADT)の期間:無作為割り付け試験(第三相試験)
*重粒子線治療後、ADTを継続しているものですが、なるべく早く内分泌療法をやめていただけるよう論文をいろいろ当たっています。
<抄録>
背景:局所限局性の高リスク前立腺癌に対しては、長期のADTに放射線治療を組み合わせるのが標準的治療であるが、ADTの至適期間については一定のコンセンサスはない。
目的:放射線治療に加えてADTをそれぞれ36か月、18か月施行した2群の治療成績を比較し、ADTの必要期間について検討。
方法:2000年から2008年まで、630例の高リスク局所限局前立腺癌患者を2群に割り付け。骨盤、前立腺照射+36か月のADTを施行する310例(long arm)と同様の放射線照射に18か月のADTを行う320例(short arm)で検討した。
予後判定:全生存(overall survival OS)及び生存の質(quality of life QOL)を指標とした。
結果:平均9.4年の経過観察で、290人が死亡した(long arm 147人、short arm143人)
5年OSはlong arm91% short arm86%で統計的有意差はなかった。QOLではshort armが有意に優った。
結論:局所限局高リスク前立腺癌に対する放射線治療とADTの組み合わせでは、36か月間のADTは18か月のADTに対して有意な上乗せ効果はなかった。症例を選べば、ADTを18か月に短縮し、QOLを落とすことなく同等の成績を得ることが可能と思われた。
<コメント>読んだのは抄録のみで、高リスク群の具体的な内容、放射線治療の内容が不明なこと、かなり以前の治療例であることなどが、マイナスポイントですが、いたずらに長くホルモン治療をするのが必ずしもいいわけではないとする報告と理解。
Eur Urol. 2018 Oct;74(4):432-441. doi: 10.1016/j.eururo.2018.06.018.
高リスク前立腺癌患者における内分泌療法(ADT)の期間:無作為割り付け試験(第三相試験)
*重粒子線治療後、ADTを継続しているものですが、なるべく早く内分泌療法をやめていただけるよう論文をいろいろ当たっています。
<抄録>
背景:局所限局性の高リスク前立腺癌に対しては、長期のADTに放射線治療を組み合わせるのが標準的治療であるが、ADTの至適期間については一定のコンセンサスはない。
目的:放射線治療に加えてADTをそれぞれ36か月、18か月施行した2群の治療成績を比較し、ADTの必要期間について検討。
方法:2000年から2008年まで、630例の高リスク局所限局前立腺癌患者を2群に割り付け。骨盤、前立腺照射+36か月のADTを施行する310例(long arm)と同様の放射線照射に18か月のADTを行う320例(short arm)で検討した。
予後判定:全生存(overall survival OS)及び生存の質(quality of life QOL)を指標とした。
結果:平均9.4年の経過観察で、290人が死亡した(long arm 147人、short arm143人)
5年OSはlong arm91% short arm86%で統計的有意差はなかった。QOLではshort armが有意に優った。
結論:局所限局高リスク前立腺癌に対する放射線治療とADTの組み合わせでは、36か月間のADTは18か月のADTに対して有意な上乗せ効果はなかった。症例を選べば、ADTを18か月に短縮し、QOLを落とすことなく同等の成績を得ることが可能と思われた。
<コメント>読んだのは抄録のみで、高リスク群の具体的な内容、放射線治療の内容が不明なこと、かなり以前の治療例であることなどが、マイナスポイントですが、いたずらに長くホルモン治療をするのが必ずしもいいわけではないとする報告と理解。
nadir PSA
投稿者:ぽんた 投稿日:2020/08/20(木) 09:50:19 No.69
Nadir PSA is a strong predictor of treatment outcome in intermediate and high risk localized prostate cancer patients treated by definitive external beam radiotherapy and androgen deprivation
Fady B. Geara, Muhammad Bulbul, Raja B. Khauli, Therese Y. Andraos, Mirna Abboud, Abdelatif Al Mousa, Nasim Sarhan, Ahmed Salem, Hamza Ghatasheh, Anoud Alnsour, Zeina Ayoub, Ibrahim Abu Gheida, Maya Charafeddine, Mohammed Shahait, Ali Shamseddine, Rami Abu Gheida & Jamal Khader
Radiation Oncology volume 12, Article number: 149 (2017)
高リスク、中間リスクの前立腺癌に対するADT,体外照射併用療法
- 強力な予後予測因子としてのnadir PSA -
*連投で申し訳ありません。ホルモン治療を短期で切り上げる口実を探している者です。
レバノンからの論文です。
<対象、方法>
1995年から2015年までの間、NCCN基準で中間リスク、高リスクと診断され、ADT+体外照射を行った375例の局所限局前立腺患者が対象。ADTの平均期間は10か月(3~36か月)、照射線量の平均は72Gy(70~78Gy)、経過観察期間の平均は5.8年(0.8~16.39年)、研究の終了点は生化学的再発(biochemical disease free survival:BFS)
<結果>
1. 42例(12.5%)が経過観察期間中に生化学的再発(biochemical recurrence: BCR)
2.単変量解析では治療前PSA(baseline PSA:bPSA), T-stage, グリソンスコア(GS)、照射線量、PSAの照射前値、経過中のPSA最低値(nadir PSA:nPSA)が、転帰と相関
3.ROC curve(receiver operating characteristic:ROC)では、nPSA値として0.06ng/mlが良好なBCR予測と相関
4.多変量解析ではT-stage, GS, nRSAが独立した要因としてBCRと有意に相関。bPSA,放射線量は有意差なし。
<結論>
nadirPSA 0.06という値が生化学的再発の予測に非常に有用である。
<コメント>放射線治療 with/without ADTについては治療経過中のPSAの変化が予後と相関するという報告はたくさんあり、照射前のPSA.nPSA, PSA値が半減するまでの時間などいろいろ報告があります。いずれにしてもPSAがより速やかに、より強く低下する症例が予後がいいという結論にかわりはないようです。
Fady B. Geara, Muhammad Bulbul, Raja B. Khauli, Therese Y. Andraos, Mirna Abboud, Abdelatif Al Mousa, Nasim Sarhan, Ahmed Salem, Hamza Ghatasheh, Anoud Alnsour, Zeina Ayoub, Ibrahim Abu Gheida, Maya Charafeddine, Mohammed Shahait, Ali Shamseddine, Rami Abu Gheida & Jamal Khader
Radiation Oncology volume 12, Article number: 149 (2017)
高リスク、中間リスクの前立腺癌に対するADT,体外照射併用療法
- 強力な予後予測因子としてのnadir PSA -
*連投で申し訳ありません。ホルモン治療を短期で切り上げる口実を探している者です。
レバノンからの論文です。
<対象、方法>
1995年から2015年までの間、NCCN基準で中間リスク、高リスクと診断され、ADT+体外照射を行った375例の局所限局前立腺患者が対象。ADTの平均期間は10か月(3~36か月)、照射線量の平均は72Gy(70~78Gy)、経過観察期間の平均は5.8年(0.8~16.39年)、研究の終了点は生化学的再発(biochemical disease free survival:BFS)
<結果>
1. 42例(12.5%)が経過観察期間中に生化学的再発(biochemical recurrence: BCR)
2.単変量解析では治療前PSA(baseline PSA:bPSA), T-stage, グリソンスコア(GS)、照射線量、PSAの照射前値、経過中のPSA最低値(nadir PSA:nPSA)が、転帰と相関
3.ROC curve(receiver operating characteristic:ROC)では、nPSA値として0.06ng/mlが良好なBCR予測と相関
4.多変量解析ではT-stage, GS, nRSAが独立した要因としてBCRと有意に相関。bPSA,放射線量は有意差なし。
<結論>
nadirPSA 0.06という値が生化学的再発の予測に非常に有用である。
<コメント>放射線治療 with/without ADTについては治療経過中のPSAの変化が予後と相関するという報告はたくさんあり、照射前のPSA.nPSA, PSA値が半減するまでの時間などいろいろ報告があります。いずれにしてもPSAがより速やかに、より強く低下する症例が予後がいいという結論にかわりはないようです。
京大病院の放射線治療+ADT
投稿者:ぽんた 投稿日:2020/08/21(金) 20:59:38 No.70
Long-term Outcomes of Dynamic Conformal Arc Irradiation
Combined with Neoadjuvant Hormonal Therapy in Japanese
Patients with T1c-T2N0M0 Prostate Cancer: Case Series Study
Jpn J Clin Oncol 2014;44(2)180 ? 185
京大放射線科からの論文
直接的には三次元原体照射という現在ではもはや最先端ではない方法の治療成績を示した報告ですが、自分にとって特筆すべきはGS:8であっても、neoadjuvant ADT以外は追加のADTを行わず照射終了で治療を終えていることです。
目的:T1c-T2N0M0の局所限局前立腺癌患者に対するneoadjuvant HT併用3次元原体照射の長期成績の検討。
方法:2003年3月から2007年8月まで、初回治療として3D原体照射を行った150例の日本人T1c-T2N0M0患者を対象とした。対照患者のうち、GS以上は24例/150例、
リスク分類では高リスク群が50例/150例
照射前のホルモン治療は平均6か月、照射線量の平均は74Gy.Salvage hormonal therapyはPSA値が漸増し4ng/mlを越えるまで行わなかったと。
結果:平均79か月の経過観察。Salvage hormonal therapyは10例で施行。施行時の平均PSAは4.7ng/ml。 5年生化学的非再発率、salvage hormonal therapy-free率、生存率はそれぞれ83.3%, 94.3%,96.4%
コメント:高リスク群が150例中50例もあることを勘案すると、まずまずの成績であり、
また生化学的再発をきたしsalvageホルモン療法が必要であった率を見ると、
低リスク群:0%
中間リスク群:0.5%
高リスク群:11.2 % であったとしている。すなわち高リスク群であっても放射線治療終了で治療を終えたとしても、5年間のfollowでADTが必要となるのはおおよそ10人に1人だったと理解。
放射線治療後、2年3年と長々とADTを行った検討では、経過観察の開始は通常放射線治療終了時であり、5年程度の観察期間であれば、そのうち2~3年はホルモン治療をしているわけで、これをconcurrent ADTを行わない今回のような検討と直接比較するのはフェアではないのではないかと感じています。高リスク群に対する放射線治療+ADTのランダム化比較試験でADTの期間設定として多いのは、24か月あたりの群と6か月あたりの2群に割り付けるのが多いと思われます。ただどちらの群も、経過観察の開始は放射線治療終了時であり、5年の経過観察では半分近くまだADT継続中ということになり、この比較は妥当なのかなあと思ってしまいます。
京大病院では現在も限局癌では高リスクでもneoadjuvant以外のADTは行っていないのでしょうか。
Combined with Neoadjuvant Hormonal Therapy in Japanese
Patients with T1c-T2N0M0 Prostate Cancer: Case Series Study
Jpn J Clin Oncol 2014;44(2)180 ? 185
京大放射線科からの論文
直接的には三次元原体照射という現在ではもはや最先端ではない方法の治療成績を示した報告ですが、自分にとって特筆すべきはGS:8であっても、neoadjuvant ADT以外は追加のADTを行わず照射終了で治療を終えていることです。
目的:T1c-T2N0M0の局所限局前立腺癌患者に対するneoadjuvant HT併用3次元原体照射の長期成績の検討。
方法:2003年3月から2007年8月まで、初回治療として3D原体照射を行った150例の日本人T1c-T2N0M0患者を対象とした。対照患者のうち、GS以上は24例/150例、
リスク分類では高リスク群が50例/150例
照射前のホルモン治療は平均6か月、照射線量の平均は74Gy.Salvage hormonal therapyはPSA値が漸増し4ng/mlを越えるまで行わなかったと。
結果:平均79か月の経過観察。Salvage hormonal therapyは10例で施行。施行時の平均PSAは4.7ng/ml。 5年生化学的非再発率、salvage hormonal therapy-free率、生存率はそれぞれ83.3%, 94.3%,96.4%
コメント:高リスク群が150例中50例もあることを勘案すると、まずまずの成績であり、
また生化学的再発をきたしsalvageホルモン療法が必要であった率を見ると、
低リスク群:0%
中間リスク群:0.5%
高リスク群:11.2 % であったとしている。すなわち高リスク群であっても放射線治療終了で治療を終えたとしても、5年間のfollowでADTが必要となるのはおおよそ10人に1人だったと理解。
放射線治療後、2年3年と長々とADTを行った検討では、経過観察の開始は通常放射線治療終了時であり、5年程度の観察期間であれば、そのうち2~3年はホルモン治療をしているわけで、これをconcurrent ADTを行わない今回のような検討と直接比較するのはフェアではないのではないかと感じています。高リスク群に対する放射線治療+ADTのランダム化比較試験でADTの期間設定として多いのは、24か月あたりの群と6か月あたりの2群に割り付けるのが多いと思われます。ただどちらの群も、経過観察の開始は放射線治療終了時であり、5年の経過観察では半分近くまだADT継続中ということになり、この比較は妥当なのかなあと思ってしまいます。
京大病院では現在も限局癌では高リスクでもneoadjuvant以外のADTは行っていないのでしょうか。
放射線治療前のPSAの下がり方のいい症例
投稿者:ぽんた 投稿日:2020/03/14(土) 20:50:13 No.66
[返信]
Achieving PSA?<?0.2?ng/ml before Radiation Therapy Is a Strong Predictor of Treatment Success in Patients with High-Risk Locally Advanced Prostate Cancer
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6854218/
重粒子線治療前のネオアジュバントADT(アンドロゲン除去療法)として、ビカルタミドとリュープリンによる
治療を始めて約3か月、先日の検診でPSA値が0.08ng/mlと著明に低下しているのが嬉しくて、
今回の論文を紹介させていただきます。
このような論文の紹介を不快と思われる方もおられるかも知れませんが、ご容赦ねがいます。
筆頭著者は新潟大学泌尿器科、共著者に放射線科の先生が名前を連ねています。
ハイリスクの局所進行性前立腺癌に対する放射線治療(外照射)について、
治療前のホルモン療法でPSA値が0.2ng/ml以下になることが、
良好な予後を得るうえでの指標であったとの論文です。
<対象>
2005年から2010年の5年間で、PSA 20ng>ml または グリソンスコア 8以上
または 臨床病期 3a以上の204人のハイリスク患者204人に対して、ADT を併用した放射線治療を施行。
ネオアジュバントADTはLH-RHアゴニスト単独、または抗アンドロゲン剤との併用で、平均7か月、
トータルのADT期間の平均は27か月。放射線治療は3次元原体照射で70Gyを35分割で。
経過観察の平均は113か月
<結果>
PSA生化学的非再発率、がん特異的生存率、全生存率は5年で、84.1%, 98.5%, 93.6%
10年で67.9%, 91.2%, 78.1%という成績。
外照射前のPSA<0.2ng/ml でPSA生化学的非再発率、がん特異的生存率、全生存率が有意に良好。
多変量解析では(1)70歳以上(2)放射線治療前のPSA>0.2ng/mlが転帰不良の要因であった。
診断時のPSA, 臨床病期、グリソンスコア、ハイリスク要因の数、ADT期間は治療成績と相関せず。
<コメント>
この論文以外にも、ネオアジュバントATDによく反応してPSAの値の下がりがいい症例は
放射線治療の成績がいいとする論文は多いとのことです。
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6854218/
重粒子線治療前のネオアジュバントADT(アンドロゲン除去療法)として、ビカルタミドとリュープリンによる
治療を始めて約3か月、先日の検診でPSA値が0.08ng/mlと著明に低下しているのが嬉しくて、
今回の論文を紹介させていただきます。
このような論文の紹介を不快と思われる方もおられるかも知れませんが、ご容赦ねがいます。
筆頭著者は新潟大学泌尿器科、共著者に放射線科の先生が名前を連ねています。
ハイリスクの局所進行性前立腺癌に対する放射線治療(外照射)について、
治療前のホルモン療法でPSA値が0.2ng/ml以下になることが、
良好な予後を得るうえでの指標であったとの論文です。
<対象>
2005年から2010年の5年間で、PSA 20ng>ml または グリソンスコア 8以上
または 臨床病期 3a以上の204人のハイリスク患者204人に対して、ADT を併用した放射線治療を施行。
ネオアジュバントADTはLH-RHアゴニスト単独、または抗アンドロゲン剤との併用で、平均7か月、
トータルのADT期間の平均は27か月。放射線治療は3次元原体照射で70Gyを35分割で。
経過観察の平均は113か月
<結果>
PSA生化学的非再発率、がん特異的生存率、全生存率は5年で、84.1%, 98.5%, 93.6%
10年で67.9%, 91.2%, 78.1%という成績。
外照射前のPSA<0.2ng/ml でPSA生化学的非再発率、がん特異的生存率、全生存率が有意に良好。
多変量解析では(1)70歳以上(2)放射線治療前のPSA>0.2ng/mlが転帰不良の要因であった。
診断時のPSA, 臨床病期、グリソンスコア、ハイリスク要因の数、ADT期間は治療成績と相関せず。
<コメント>
この論文以外にも、ネオアジュバントATDによく反応してPSAの値の下がりがいい症例は
放射線治療の成績がいいとする論文は多いとのことです。
放射線(小線源)治療における射精機能への影響
投稿者:羊毛 投稿日:2019/10/17(木) 23:29:59 No.65
[返信]
小線源治療では性機能は摘出手術と比べて残ると言われてますが、射精機能については「ドライになってしまう」という話と「量が少なくなる」という話があり、論文等があるかどうか調べてみようと思い、検索してみました。
まずは日本語のページから。(「前立腺癌 小線源療法 精液はどうなる」で検索)
-----
「がん情報サービス-前立腺がん」
「5.放射線治療」→「2)組織内照射療法(密封小線源療法)」に次の記述があります。
(引用開始)
また、年齢にもよりますが、外照射療法に比べて性機能が維持される割合が高いことが特徴です。ただし、精液の量は減少します。』
(引用終了)
-----
「順天堂大学 第7回市民公開講座 質疑応答:講演3」
(引用開始)
Q.がん治療に密封小線源治療(brachytherapy)をした後には、前立腺の精液作成はどうなるのですか。
A.
1. SEED後に無精液を生じる確率は25%との報告があります。
2. 大半の症例で精液量減少の訴えが報告されています。
3. 5-6年の経過で、ごく少量の漿液性のものを排出するようになるというのが多いようです。
4. 排出量についての詳細な記述は、検索した限りでは見当たりませんでした。
5. 精液産生の工場が破壊されるため、必然の結果ではあります。
6. 精嚢の末端に一部産生能が残存するため、少量はできるとされています。
7. 射精管が閉塞するため排出不能となるということも言われています。』
(引用終了)
-----
...(続きを読む)
まずは日本語のページから。(「前立腺癌 小線源療法 精液はどうなる」で検索)
-----
「がん情報サービス-前立腺がん」
「5.放射線治療」→「2)組織内照射療法(密封小線源療法)」に次の記述があります。
(引用開始)
また、年齢にもよりますが、外照射療法に比べて性機能が維持される割合が高いことが特徴です。ただし、精液の量は減少します。』
(引用終了)
-----
「順天堂大学 第7回市民公開講座 質疑応答:講演3」
(引用開始)
Q.がん治療に密封小線源治療(brachytherapy)をした後には、前立腺の精液作成はどうなるのですか。
A.
1. SEED後に無精液を生じる確率は25%との報告があります。
2. 大半の症例で精液量減少の訴えが報告されています。
3. 5-6年の経過で、ごく少量の漿液性のものを排出するようになるというのが多いようです。
4. 排出量についての詳細な記述は、検索した限りでは見当たりませんでした。
5. 精液産生の工場が破壊されるため、必然の結果ではあります。
6. 精嚢の末端に一部産生能が残存するため、少量はできるとされています。
7. 射精管が閉塞するため排出不能となるということも言われています。』
(引用終了)
-----
...(続きを読む)
治療後の排尿症状について
投稿者:眞 投稿日:2018/08/17(金) 13:57:29 No.64
[返信]
治療後の頻尿などの排尿症状についていままであげた二つの以下の論文よりグラフを示し、もう少し詳しく書いてみます。
1.東京大学の山本健太郎氏の博士論文コーンビムCTによる画像誘導放射線治療を併用した前立腺癌に対する強度変調回転照射の検討 以下山本論文とよびます。
2.第29回前立腺シンポジウムで発表された奈良県立医科大学の田中宣道氏他のIPSSを用いた排尿症状改善からみた至適根治治療法選択 泌尿器外科 2014;27(8): 1301-1304 以下田中論文とよびます。
山本論文では「尿路系有害事象」、田中論文では「排尿症状」と書かれていますが、ここでは「排尿症状」という言葉を用います。
IPSSの説明は山本論文より転記します。
IPSS(International Prostate Symptom Score)
排尿症状の評価法として、世界的に広く使用されている評価尺度であり、信頼性・妥当性が検証済みである。IPSSの内容は、蓄尿症状3項目(頻尿・夜間頻尿・尿意切迫感)、排尿症状3項目(尿線途絶、尿勢低下、腹圧排尿)、排尿後症状1項目(残尿感)、QOLの計8項目である。
・IPSS
スコアが高い方が重症です。
山本論文での患者の内訳は以下のとおり。
0-7点( mild )の患 者が 109 名( 67.2% )
8-19 点 (moderate )の患者が 72 名( 25.1% )
20 -35 点 (severe severe) の患者が 22 名( 7.7% )
以下のように書かれています。
この 3群で層別化を行い、治療前の 群で層別化を行い、治療前の 群で層別化を行い、治療前の IPSSを基準と したときの変化を図Ⅳ-1に示す。観察期間中の IPSSの変動中央値は、 mild / moderate / severe 群で各々 群で各々 4.5 / 5.0 / -3.5 であり( p < 0.01 )、治療前の IPSSが高い群 ( sever )では、低い群( mild, moderate )と比較し、治療後の IPSSは悪化せずむしろ改善している傾向がみられた。
さらに図Ⅳ -2を示し以下のように書かれています。
大多数の症例で、 IPSSは治療後約 3ヶ月で治療前の水準まで改善した。
...(続きを読む)
1.東京大学の山本健太郎氏の博士論文コーンビムCTによる画像誘導放射線治療を併用した前立腺癌に対する強度変調回転照射の検討 以下山本論文とよびます。
2.第29回前立腺シンポジウムで発表された奈良県立医科大学の田中宣道氏他のIPSSを用いた排尿症状改善からみた至適根治治療法選択 泌尿器外科 2014;27(8): 1301-1304 以下田中論文とよびます。
山本論文では「尿路系有害事象」、田中論文では「排尿症状」と書かれていますが、ここでは「排尿症状」という言葉を用います。
IPSSの説明は山本論文より転記します。
IPSS(International Prostate Symptom Score)
排尿症状の評価法として、世界的に広く使用されている評価尺度であり、信頼性・妥当性が検証済みである。IPSSの内容は、蓄尿症状3項目(頻尿・夜間頻尿・尿意切迫感)、排尿症状3項目(尿線途絶、尿勢低下、腹圧排尿)、排尿後症状1項目(残尿感)、QOLの計8項目である。
・IPSS
スコアが高い方が重症です。
山本論文での患者の内訳は以下のとおり。
0-7点( mild )の患 者が 109 名( 67.2% )
8-19 点 (moderate )の患者が 72 名( 25.1% )
20 -35 点 (severe severe) の患者が 22 名( 7.7% )
以下のように書かれています。
この 3群で層別化を行い、治療前の 群で層別化を行い、治療前の 群で層別化を行い、治療前の IPSSを基準と したときの変化を図Ⅳ-1に示す。観察期間中の IPSSの変動中央値は、 mild / moderate / severe 群で各々 群で各々 4.5 / 5.0 / -3.5 であり( p < 0.01 )、治療前の IPSSが高い群 ( sever )では、低い群( mild, moderate )と比較し、治療後の IPSSは悪化せずむしろ改善している傾向がみられた。
さらに図Ⅳ -2を示し以下のように書かれています。
大多数の症例で、 IPSSは治療後約 3ヶ月で治療前の水準まで改善した。
...(続きを読む)
奥井識仁(おくい・ひさひと)(よこすか女性泌尿器科・泌尿器科クリニック院長)先生の論文を紹介します。
運動をするとCRPC(去勢抵抗性前立腺がん)にならない?
前立腺がんの患者さんがCRPCにならないためには、どうすればよいのでしょうか。
私は15年以上前から、運動がリスクを下げるのではないかと考えていました。
それを裏付ける論文が、11年にハーバード大学から発表されました。
その研究によると、1週間に3時間以上、ランニング、水泳、テニスといった激しい運動をした人は、1時間未満の人と比べて、前立腺がんによる死亡リスクが61%低いというのです。
また、ハーバード大学の別の研究者たちが11年に発表した論文でも、運動が前立腺がんを抑制することが報告されています。
その研究によると、週3時間未満「楽なペースの散歩」をした人がCRPCになるリスクを1.0とした場合、週3時間以上「早歩きの散歩」をした人のリスクは0.43倍になるといいます。
これらの運動について考えてみましょう。
60代前半の男性は1時間で7~8km走ることができます。
3時間の運動なら21~24km。1カ月(30日)では、90~102kmです。
日常生活での運動量を加えると、1週間に3時間の激しい運動をする人は、1カ月に100~120kmの運動をしていることになります。
また、60代前半の男性は1時間早歩きをすると、5~6km歩けます。
週3時間だと15~18km、1カ月では64~77kmに当たります。日常生活での運動量を加えると、週3時間早歩きをする人は1カ月に90~110kmの運動をしていることになります。
前立腺がん死を防ぐ1カ月の移動距離は?
私も18年、Juntendo Medical Journalに、前立腺がんによる死亡が運動によって抑えられるという論文を発表しました。
102人の前立腺がんの患者さん(平均74.8歳)について、前立腺がんと告知してからの8年間について調べてみました。どの患者さんも、すでに手術できるような状態でなく、ホルモン療法をしています。
みなさん高齢で、1時間ランニングするような運動はできませんから、暇があれば万歩計を付けて外出し、少しずつでも早歩きをしていただくよう指導しました。
すると、1カ月120km以上歩いた患者さんと120km未満の患者さんが、ちょうど51人ずつに分かれました。
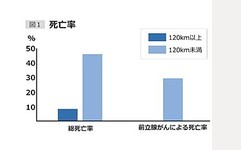
図1を見てください。左側のグラフは、「総死亡率」を表しています。
総死亡率とは、ある集団の中で亡くなった人の割合を示し、前立腺がんだけでなく、脳梗塞(こうそく)、胃がん、心筋梗塞などさまざまな死亡原因が含まれます。
8年間で48人が亡くなったのですが、120km以上の早歩きをしているグループは31%(16人)、それ未満の人は63%(32人)でした。
120km以上の早歩きをしているグループは、総死亡率が低いことが分かります。
右側のグラフは前立腺がんによる死亡率を表しています。
120km以上の早歩きをしているグループには前立腺がんによる死亡者はいませんでした。
...(続きを読む)
運動をするとCRPC(去勢抵抗性前立腺がん)にならない?
前立腺がんの患者さんがCRPCにならないためには、どうすればよいのでしょうか。
私は15年以上前から、運動がリスクを下げるのではないかと考えていました。
それを裏付ける論文が、11年にハーバード大学から発表されました。
その研究によると、1週間に3時間以上、ランニング、水泳、テニスといった激しい運動をした人は、1時間未満の人と比べて、前立腺がんによる死亡リスクが61%低いというのです。
また、ハーバード大学の別の研究者たちが11年に発表した論文でも、運動が前立腺がんを抑制することが報告されています。
その研究によると、週3時間未満「楽なペースの散歩」をした人がCRPCになるリスクを1.0とした場合、週3時間以上「早歩きの散歩」をした人のリスクは0.43倍になるといいます。
これらの運動について考えてみましょう。
60代前半の男性は1時間で7~8km走ることができます。
3時間の運動なら21~24km。1カ月(30日)では、90~102kmです。
日常生活での運動量を加えると、1週間に3時間の激しい運動をする人は、1カ月に100~120kmの運動をしていることになります。
また、60代前半の男性は1時間早歩きをすると、5~6km歩けます。
週3時間だと15~18km、1カ月では64~77kmに当たります。日常生活での運動量を加えると、週3時間早歩きをする人は1カ月に90~110kmの運動をしていることになります。
前立腺がん死を防ぐ1カ月の移動距離は?
私も18年、Juntendo Medical Journalに、前立腺がんによる死亡が運動によって抑えられるという論文を発表しました。
102人の前立腺がんの患者さん(平均74.8歳)について、前立腺がんと告知してからの8年間について調べてみました。どの患者さんも、すでに手術できるような状態でなく、ホルモン療法をしています。
みなさん高齢で、1時間ランニングするような運動はできませんから、暇があれば万歩計を付けて外出し、少しずつでも早歩きをしていただくよう指導しました。
すると、1カ月120km以上歩いた患者さんと120km未満の患者さんが、ちょうど51人ずつに分かれました。
図1を見てください。左側のグラフは、「総死亡率」を表しています。
総死亡率とは、ある集団の中で亡くなった人の割合を示し、前立腺がんだけでなく、脳梗塞(こうそく)、胃がん、心筋梗塞などさまざまな死亡原因が含まれます。
8年間で48人が亡くなったのですが、120km以上の早歩きをしているグループは31%(16人)、それ未満の人は63%(32人)でした。
120km以上の早歩きをしているグループは、総死亡率が低いことが分かります。
右側のグラフは前立腺がんによる死亡率を表しています。
120km以上の早歩きをしているグループには前立腺がんによる死亡者はいませんでした。
...(続きを読む)
トリモダリティ治療の晩期障害
投稿者:SANZOKU 投稿日:2018/02/06(火) 22:27:04 No.62
[返信]
晩期障害は治療後10年経過しても発症することがあるようですが、
一般に1年~3年が好発時期らしいです。
特に1年3ヶ月くらいにピークを迎えます。
私は2年半前にトリモダリティ治療の外部照射を終えました。
その後、1年4ヶ月後に血便、2年後に血尿と、晩期障害と思われる症状を経験しました。
ここにその経過を報告します。
私は超ハイリスクだったため、全骨盤照射という外部照射を行いました。
通常は前立腺と精嚢を対象とするのですが、骨盤内リンパ節も対象とする照射です。
そのためやや強めの晩期障害を経験することになりました。
血便、血尿の両方を経験している人は少ないと思います。
<血便>
急性期の症状は、外部照射開始3日目から下痢が始まりガスも多くなる。
照射を重ねるに連れ悪化して,照射末期は6回/日の頻便である。
とにかくお腹が重苦しい。
照射を終了して1週間するとお腹の重苦しさは軽くなってきた。
その後も改善し、2ヶ月で1~3回/日となるが、ガスはやや多く不安定。
その後は調子の波はあるが、ゆっくりと改善する。
血便は1年4ヶ月後、お腹の調子が少し低調になった際に突然始まる。
結局1年9ヶ月後を最後にして全部で6回確認。
毎度便の最後に数cmの塊が確認される。
お腹の重苦しさ、軟便、ガス便などが感じられる時に発生。
お腹の調子に波はあるが、現在(2年半後)は
急性期の症状が最も緩和された時のレベルまで改善。
対処法としてはお腹の調子が悪いときは、消化の良い物を食する、
...(続きを読む)
一般に1年~3年が好発時期らしいです。
特に1年3ヶ月くらいにピークを迎えます。
私は2年半前にトリモダリティ治療の外部照射を終えました。
その後、1年4ヶ月後に血便、2年後に血尿と、晩期障害と思われる症状を経験しました。
ここにその経過を報告します。
私は超ハイリスクだったため、全骨盤照射という外部照射を行いました。
通常は前立腺と精嚢を対象とするのですが、骨盤内リンパ節も対象とする照射です。
そのためやや強めの晩期障害を経験することになりました。
血便、血尿の両方を経験している人は少ないと思います。
<血便>
急性期の症状は、外部照射開始3日目から下痢が始まりガスも多くなる。
照射を重ねるに連れ悪化して,照射末期は6回/日の頻便である。
とにかくお腹が重苦しい。
照射を終了して1週間するとお腹の重苦しさは軽くなってきた。
その後も改善し、2ヶ月で1~3回/日となるが、ガスはやや多く不安定。
その後は調子の波はあるが、ゆっくりと改善する。
血便は1年4ヶ月後、お腹の調子が少し低調になった際に突然始まる。
結局1年9ヶ月後を最後にして全部で6回確認。
毎度便の最後に数cmの塊が確認される。
お腹の重苦しさ、軟便、ガス便などが感じられる時に発生。
お腹の調子に波はあるが、現在(2年半後)は
急性期の症状が最も緩和された時のレベルまで改善。
対処法としてはお腹の調子が悪いときは、消化の良い物を食する、
...(続きを読む)
北里大学の津村秀康氏他の論文、Impact of five-tiered Gleason grade groups on prognostic prediction in clinical stage T3 prostate cancer undergoing high-dose-rate brachytherapy.の概要を紹介します。
なお、表題に示されています ISUPで承認されたGSの新しいグレード分類による報告は煩雑になりますので省略します。
・2003年11月から2012年12月のT3a 203人、T3b 80人計283人が対象
・HDRは平均D90 PTV線量: 7.5Gy/1分割 を5回実施、また、外照射は1回3Gy を10回照射
・ホルモン治療はすべての患者に術前に6か月以上、外照射の後に3年実施
・10年PSA非再発率は以下のとおり。
T3a 79%
T3b 64%
・10年癌特異的生存率は以下のとおり
T3a 96%
T3b 91%
なお、表題に示されています ISUPで承認されたGSの新しいグレード分類による報告は煩雑になりますので省略します。
・2003年11月から2012年12月のT3a 203人、T3b 80人計283人が対象
・HDRは平均D90 PTV線量: 7.5Gy/1分割 を5回実施、また、外照射は1回3Gy を10回照射
・ホルモン治療はすべての患者に術前に6か月以上、外照射の後に3年実施
・10年PSA非再発率は以下のとおり。
T3a 79%
T3b 64%
・10年癌特異的生存率は以下のとおり
T3a 96%
T3b 91%
手術後のadjuvant radiotherapy に関して検索していたところ、次の論文をみいだしたので紹介します。
・Indian J Urol. 2017 Jan-Mar;33(1):64-69.
独立行政法人 国立病院機構 九州がんセンターの泌尿器科の古林伸紀氏を筆頭著者とする論文です。
1998年8月から2013年5月の間に九州がんセンターまたは関連病院で手術を受けた481人の患者が対象であり、内訳はD'Amico のリスク分類 により低リスクは107人、中間リスクは222人、高リスクは152人であり、5年PSA非再発率は以下のとおり。
低リスク 96.5%
中間リスク 88.9%
高リスク 72.6%
中間リスクの因子の数によりPSA非再発率は以下のとおり。
1 94.9%
2 88.4%
3 49.0%
abstract の結論には以下のように書かれています。
Patients classified into the intermediate-risk group based on all
three intermediate risk factors are less likely to achieve a complete
cure through surgery alone.
Google翻訳
3つの中間リスク因子すべてに基づいて中リスク群に分類される患者は、
手術単独で完全治癒を達成する可能性は低い。
なお、骨盤リンパ節郭清を実施したと書かれています。
サイトの治療法比較3にこの論文のデータを追記しました。
D'Amico のリスク分類を使用しているのはそう多くないですが、例えば、10 の奈良県立医科大学の小線源の論文はD'Amicoであり、と比較してみます。
...(続きを読む)
・Indian J Urol. 2017 Jan-Mar;33(1):64-69.
独立行政法人 国立病院機構 九州がんセンターの泌尿器科の古林伸紀氏を筆頭著者とする論文です。
1998年8月から2013年5月の間に九州がんセンターまたは関連病院で手術を受けた481人の患者が対象であり、内訳はD'Amico のリスク分類 により低リスクは107人、中間リスクは222人、高リスクは152人であり、5年PSA非再発率は以下のとおり。
低リスク 96.5%
中間リスク 88.9%
高リスク 72.6%
中間リスクの因子の数によりPSA非再発率は以下のとおり。
1 94.9%
2 88.4%
3 49.0%
abstract の結論には以下のように書かれています。
Patients classified into the intermediate-risk group based on all
three intermediate risk factors are less likely to achieve a complete
cure through surgery alone.
Google翻訳
3つの中間リスク因子すべてに基づいて中リスク群に分類される患者は、
手術単独で完全治癒を達成する可能性は低い。
なお、骨盤リンパ節郭清を実施したと書かれています。
サイトの治療法比較3にこの論文のデータを追記しました。
D'Amico のリスク分類を使用しているのはそう多くないですが、例えば、10 の奈良県立医科大学の小線源の論文はD'Amicoであり、と比較してみます。
...(続きを読む)
トリモダリティの外照射終了後2年
投稿者:SANZOKU 投稿日:2017/07/27(木) 23:14:29 No.59
[返信]
概要
自分には、この病が発覚する前から前立腺周辺にいろいろ症状がありました。
https://sen-you.boy.jp/bbs/main/index.cgi?res=4214
それは両下腹部、肛門、仙骨周辺、臀部、鼠径部、バットなどに感ずる鈍痛、痺れ、掻痒感、拍動、違和感などです。
山や谷がありますが、それらは治療中も治療後も続いていました。しかし治療後1年半後くらいから影を潜めるようになり、現在では若干の名残はあるもののほぼ消失しました。このことからこれらがこの病気の症状であったと確信を抱くようになりました。
その代わりに治療後に出現したものもあります。それは血便や頻便といった直腸症状、血尿などの排尿症状、皮膚炎などです。これらは治療に伴って現れた症状だと思います。ただ現在のところ日常生活に支障をきたす程ではありません。
PSAの推移ですが、今回(今年の1月の値)は0.267で、その3ヶ月前が0.1999、3ヶ月後が0.256でしたから、現状はプラトーに達していることになります。
https://sen-you.boy.jp/bbs/intro/index.cgi?res=75
できれば下降に転じていてくれば良かったのですが・・・。
いよいよこれからが正念場ですね。
同時期にトリモ治療を受けた3人は数値こそ多少異なりますが、
同様の経過を辿っています。
放射線治療によると思われる症状
治療直後にはいろいろ症状がありました。
https://sen-you.boy.jp/bbs/paper/index.cgi?read=32
現在ではそのような急性期の症状は収まって、晩期障害と思われる症状が出ています。
①排尿
半年前には治療前まであと少しのところまで改善していました。ところがその頃から徐々に尿が微妙に沁みるようになってきました。最近では唸るところまでいきませんが、そこそこ沁みるようになっていました。先週気が付いたのですが、排尿の当初に少し赤い尿が出るようになりました。よく観察すると、排尿の終わりにも赤い尿が少し出ます。時に小さなゴミのような血栓も混じることがあります。これでほぼ1週間、毎日1~2回は観察されます。
このような按配なので以前より切迫感を感じることがあります。尿回数も少し増えています。しかし早めに排尿していれば、支障はほとんどありません。対策としてユリーフを飲みはじめています。排尿時の沁みが少し改善されるだけで、今のところ効果は未知数です。
同時期に入院されたヤマさんも半年前に経験され、その後3ヶ月あまりで良くなったそうなので、私もそのような経過を辿ることを期待してあまり心配していません。
②排便
半年あまり前に便の最後に少し確認できる程度の血便がありました。その後も5ヶ月間で6回確認しています。その頃はガスの排出も多く、お腹が重苦しく感じて若干元気をスポイルしている時もありました。しかし直近の3ヶ月は血便は確認されておらず、完全には復調していませんが、お腹の重苦しさは軽快しています。このまま収まってくれればと期待しています。もっと重度の症状なら、ステロイド注腸やアルゴンレーザーでの焼灼、高気圧酸素療法などの治療法もありますが、この程度なら自然に治ることが多いようです。
...(続きを読む)
自分には、この病が発覚する前から前立腺周辺にいろいろ症状がありました。
https://sen-you.boy.jp/bbs/main/index.cgi?res=4214
それは両下腹部、肛門、仙骨周辺、臀部、鼠径部、バットなどに感ずる鈍痛、痺れ、掻痒感、拍動、違和感などです。
山や谷がありますが、それらは治療中も治療後も続いていました。しかし治療後1年半後くらいから影を潜めるようになり、現在では若干の名残はあるもののほぼ消失しました。このことからこれらがこの病気の症状であったと確信を抱くようになりました。
その代わりに治療後に出現したものもあります。それは血便や頻便といった直腸症状、血尿などの排尿症状、皮膚炎などです。これらは治療に伴って現れた症状だと思います。ただ現在のところ日常生活に支障をきたす程ではありません。
PSAの推移ですが、今回(今年の1月の値)は0.267で、その3ヶ月前が0.1999、3ヶ月後が0.256でしたから、現状はプラトーに達していることになります。
https://sen-you.boy.jp/bbs/intro/index.cgi?res=75
できれば下降に転じていてくれば良かったのですが・・・。
いよいよこれからが正念場ですね。
同時期にトリモ治療を受けた3人は数値こそ多少異なりますが、
同様の経過を辿っています。
放射線治療によると思われる症状
治療直後にはいろいろ症状がありました。
https://sen-you.boy.jp/bbs/paper/index.cgi?read=32
現在ではそのような急性期の症状は収まって、晩期障害と思われる症状が出ています。
①排尿
半年前には治療前まであと少しのところまで改善していました。ところがその頃から徐々に尿が微妙に沁みるようになってきました。最近では唸るところまでいきませんが、そこそこ沁みるようになっていました。先週気が付いたのですが、排尿の当初に少し赤い尿が出るようになりました。よく観察すると、排尿の終わりにも赤い尿が少し出ます。時に小さなゴミのような血栓も混じることがあります。これでほぼ1週間、毎日1~2回は観察されます。
このような按配なので以前より切迫感を感じることがあります。尿回数も少し増えています。しかし早めに排尿していれば、支障はほとんどありません。対策としてユリーフを飲みはじめています。排尿時の沁みが少し改善されるだけで、今のところ効果は未知数です。
同時期に入院されたヤマさんも半年前に経験され、その後3ヶ月あまりで良くなったそうなので、私もそのような経過を辿ることを期待してあまり心配していません。
②排便
半年あまり前に便の最後に少し確認できる程度の血便がありました。その後も5ヶ月間で6回確認しています。その頃はガスの排出も多く、お腹が重苦しく感じて若干元気をスポイルしている時もありました。しかし直近の3ヶ月は血便は確認されておらず、完全には復調していませんが、お腹の重苦しさは軽快しています。このまま収まってくれればと期待しています。もっと重度の症状なら、ステロイド注腸やアルゴンレーザーでの焼灼、高気圧酸素療法などの治療法もありますが、この程度なら自然に治ることが多いようです。
...(続きを読む)
IMRT3年が終わって
投稿者:トム 投稿日:2017/05/31(水) 08:43:48 No.58
[返信]
トム。昭和14(1939)年生まれ、現在78歳。都内在住。高リスクIMRT患者
IMRTが終って3年
1.はじめに
最近、投稿がめっきり減ったIMRTですが、患者数が減っていることはないでしょう。IMRTを終えた方とこれから受ける方、これら声なき多くの方々に、治療終了後の一応の目安である3年‐直腸・尿路晩期障害発生率最大期間が経過したこと、加えて、個人の価値観が多様であるように掲示板にも多様な情報が有って然るべきと考え、私の体験を投稿することとしました。ご一読頂ければ幸いです。
2.がん発覚まで
・埼玉県内私立医科大学付属メディカルセンターにて、67歳から年1回、循環器内科検体検査に合わせてPSAを測定。
・2013年74歳、PSA=4.67 で同病院泌尿器科受診。生検を薦められたがMRIを希望。結果は、「右辺縁域がんの疑い。被膜外浸潤なし」
・3ヶ月後、同病院で2泊3日全身麻酔経会陰部生検。何ら不都合はなく会陰部に貼られた絆創膏にほんの少しの血痕を見ただけ。7日後、CTとPET-CT。3日後、がん告知。Gleason score(GS)=4+4、Stage=T1cM0N0、陽性率4/16。「6ヶ月後の再生検と開腹手術を決断して下さい」。当方の希望でLH-RHアゴニストと抗アンドロゲン剤の処置(ADT-CAB、1カ月製剤)。T1cは生検で発見されたというカテゴリーであり、T1cの30%はT2あるいはT3と理解していたので、実際の病期はT1cではなく、T2以上を覚悟していた。
3.IMRT、ホルモンと晩期障害
・転居に伴い同年、都内国立大学法人医学部付属病院に転院。当方が希望し、また、前主治医(准教授)が豊富な治療選択肢利用可能という理由で積極的かつ親切に薦めてくれた。准教授と相談の上、転院先の医師は指名させていただいた。セコンド・オピニオンは考えなかった。転院先選択変数は、つとに知られたその実績と片道徒歩40分の通院至便(バスや地下鉄も利用可能)。
・改めて病期判定(MRI)と病理診断。GS=4+4は同じであった。PSA=4.67, GS=4+4, Stage=T2bN0M0‐高リスクが確定。当病院泌尿器科(助教)は当初、daVinci手術を薦めたが、本から既に放射線(IMRT)の知識があったために非浸襲性治療優先を希望した。2回目(助教)、「コンファランスで治療法が決まりました、次回、教授から話があります」。3回目から当方の希望した医師に。初診から3回目まで約1か月を要した。主治医の「早く見つかって良かった、手術でも放射線でもどちらでも良い、全力を尽くします」の言葉にどれくらい助けられたか。不安も懸念も吹っ飛んだ。絶望が希望に。直ぐに放射線科を手配してくれた。
・2014年75歳、IMRT(VMAT) 2Gy x 38回=76Gy。照射は実質数分(入退室10分以内)で終了。デパートに買い物に行ったような気楽さであった。電車の時刻表の如く待ち時間は無かった。その後暫くして暗転。
・最終週3週間前(38回中24回目)から治療終了まで、徒歩から妻付き添いのタクシー通院を余儀なくされた。「宿粋」のような体の変調(宿粋は通常、照射後10日目頃から始まる不具合‐だるい、食欲が無い)、発熱(37‐38.5、照射後17時間で平熱に、このような症状聞いたことが無いと医師、遺伝的体質かと当方)、夜間排尿回数急増(3から7-8回に、1時間おきに7-8分便座に座ったまま、その都度よく眠れたが、明らかに睡眠不足)、弱い尿勢、極端な口内渇き(今でもはっきりと記憶している)などの合併症。また、治療終了直後から1週間、極端な排尿困難(出ない、閉尿寸前、代わりに汗が出る)と排便困難(出ない、粘液便が出る)。食わないから出ない、飲まないから出ないと考え直し、無理して胃に押し込んだ。尿が少しずつ出るようになり、4日経ってやっと便がでた。残尿を押し出した尿道括約筋がポンプの如く排尿を楽にしてくれた。
・まさにベッドに臥す病人であった。辛かった。体重は治療前66から58kgに(治療後3年の今、64kg前後で増え気味)。これらの症状は治療後2週間目から徐々に緩和。立ち小便が可能になった。間もなく日常生活も正常に。ふらふらの体でウオーキングを再開。
・ハルナール(排尿促進)、ベタニス(尿意制御)とガスモチン(腸管蠕動促進)を処方された。排尿最困難時にハルナールを1週間だけ服用したが、原則、薬は敬遠(薬嫌い原理主義者である)。治療終了後、処方されたガスモチンに代えてタケダ漢方胃腸薬(大黄甘草湯)を約1カ月。よく効いた。上記合併症に加えてこの期間、動悸、めまい、ふらつきがあり、ハルナールの副作用か、あるいは、放射線合併症(赤血球の減少)によるものなのか。CRP値(炎症と細胞破壊の程度を示す)の大幅上昇(IMRT直後6.45、現在0.04)に示されるように、体の不如意は、自然な生体防御反応であったと理解している。
・ホルモン治療をいつ止めるかについて率直に泌尿器科主治医に相談。定説が無いとしながらも、医師の同意を得て合計27カ月(ネオアジュバント6+コンカレント2+アジュバント19)で一旦、中止した。HbA1c>7.50のため、リュープリンの副作用である脂質代謝異常やインスリン抵抗性を懸念したため。尚、ALPや肝臓諸数値は正常であり、深刻な発汗(ホットフラッシュ)はまったく無かった。27カ月は、ADT-CAB最適期間であったと信じている(注1)。IMRT後3年、ADT-CAB効果消滅後1年5カ月の今、かさかさの頭髪、すべすべ膚と顔の皮脂は完全に原状回復、勃起と体毛(腋・腿・脛)も顕著に回復途上。乳首の発色は消えたが、ほんの少し膨らんだまま。
・晩期障害として直腸出血、血便と血尿はない。但し、この3年間(注2)、力んだ(下腹部に力を入れる、無理に押し出す)ときに数回、便にごく少量の血痕を認めた。今でも毎回、覗き込んで観察している。癖になった。排尿時に尿道に擦れるような(染みるような)感じが今でもときどきある。夜間排尿回数は、再頻値=2、平均値<2.0。治療前より減少した。但し、就寝時と起床時は含まれない。尿腺は明らかに太くなった。医師によれば、ホルモン剤は通常の前立腺肥大症薬よりはるかに強い効果がある由。便は、色、サイズや長さも改善、快便である。薬は何も使っていない。治療前最大の懸念材料であった晩期障害は楽観している。治療前のときどきの切れ痔が治療後ないのは予想外の負の後遺症。
4.PSA推移
IMRT直前(ADT-CAB5カ月後)‐ 0.02 (ホルモン高感受性と理解している)
治療中・治療後2年(ADT-CAB中断時まで)‐ <0.01
治療後2.5年ADT-CAB中断1年から現在まで3カ月毎‐ 0.02、0.04、0.08(2017年4月、ホルモン効果切れか、男性ホルモン復活の兆しか)
5.その他もろもろ
・特段の食事療法はしていない。前立腺がんで赤身脂身の牛豚肉制限(発覚前は肉が多く、魚や野菜が少なかった、若い頃から)。糖尿病対策で糖質制限努力(甘党、HbA1c≦7.00を確実に維持するため)。ミニトマトとブロッコリーだけは例外なく3食とも食卓に上る。便秘対策(便の柔らかさ調整)で牛乳かなり多めのミルクコーヒーを飲む(長期的に牛乳がこの病に良くないことは承知しているが、短期的な直腸対策を優先。勿論、カルシュウム摂取も考慮)。
・降圧剤(カルシュウム拮抗剤アムロジン2.5㎎)と血糖調整薬(メトグルコ250mg)1日1錠服用中。降圧剤は、その日の血圧次第の間欠服用。
...(続きを読む)
IMRTが終って3年
1.はじめに
最近、投稿がめっきり減ったIMRTですが、患者数が減っていることはないでしょう。IMRTを終えた方とこれから受ける方、これら声なき多くの方々に、治療終了後の一応の目安である3年‐直腸・尿路晩期障害発生率最大期間が経過したこと、加えて、個人の価値観が多様であるように掲示板にも多様な情報が有って然るべきと考え、私の体験を投稿することとしました。ご一読頂ければ幸いです。
2.がん発覚まで
・埼玉県内私立医科大学付属メディカルセンターにて、67歳から年1回、循環器内科検体検査に合わせてPSAを測定。
・2013年74歳、PSA=4.67 で同病院泌尿器科受診。生検を薦められたがMRIを希望。結果は、「右辺縁域がんの疑い。被膜外浸潤なし」
・3ヶ月後、同病院で2泊3日全身麻酔経会陰部生検。何ら不都合はなく会陰部に貼られた絆創膏にほんの少しの血痕を見ただけ。7日後、CTとPET-CT。3日後、がん告知。Gleason score(GS)=4+4、Stage=T1cM0N0、陽性率4/16。「6ヶ月後の再生検と開腹手術を決断して下さい」。当方の希望でLH-RHアゴニストと抗アンドロゲン剤の処置(ADT-CAB、1カ月製剤)。T1cは生検で発見されたというカテゴリーであり、T1cの30%はT2あるいはT3と理解していたので、実際の病期はT1cではなく、T2以上を覚悟していた。
3.IMRT、ホルモンと晩期障害
・転居に伴い同年、都内国立大学法人医学部付属病院に転院。当方が希望し、また、前主治医(准教授)が豊富な治療選択肢利用可能という理由で積極的かつ親切に薦めてくれた。准教授と相談の上、転院先の医師は指名させていただいた。セコンド・オピニオンは考えなかった。転院先選択変数は、つとに知られたその実績と片道徒歩40分の通院至便(バスや地下鉄も利用可能)。
・改めて病期判定(MRI)と病理診断。GS=4+4は同じであった。PSA=4.67, GS=4+4, Stage=T2bN0M0‐高リスクが確定。当病院泌尿器科(助教)は当初、daVinci手術を薦めたが、本から既に放射線(IMRT)の知識があったために非浸襲性治療優先を希望した。2回目(助教)、「コンファランスで治療法が決まりました、次回、教授から話があります」。3回目から当方の希望した医師に。初診から3回目まで約1か月を要した。主治医の「早く見つかって良かった、手術でも放射線でもどちらでも良い、全力を尽くします」の言葉にどれくらい助けられたか。不安も懸念も吹っ飛んだ。絶望が希望に。直ぐに放射線科を手配してくれた。
・2014年75歳、IMRT(VMAT) 2Gy x 38回=76Gy。照射は実質数分(入退室10分以内)で終了。デパートに買い物に行ったような気楽さであった。電車の時刻表の如く待ち時間は無かった。その後暫くして暗転。
・最終週3週間前(38回中24回目)から治療終了まで、徒歩から妻付き添いのタクシー通院を余儀なくされた。「宿粋」のような体の変調(宿粋は通常、照射後10日目頃から始まる不具合‐だるい、食欲が無い)、発熱(37‐38.5、照射後17時間で平熱に、このような症状聞いたことが無いと医師、遺伝的体質かと当方)、夜間排尿回数急増(3から7-8回に、1時間おきに7-8分便座に座ったまま、その都度よく眠れたが、明らかに睡眠不足)、弱い尿勢、極端な口内渇き(今でもはっきりと記憶している)などの合併症。また、治療終了直後から1週間、極端な排尿困難(出ない、閉尿寸前、代わりに汗が出る)と排便困難(出ない、粘液便が出る)。食わないから出ない、飲まないから出ないと考え直し、無理して胃に押し込んだ。尿が少しずつ出るようになり、4日経ってやっと便がでた。残尿を押し出した尿道括約筋がポンプの如く排尿を楽にしてくれた。
・まさにベッドに臥す病人であった。辛かった。体重は治療前66から58kgに(治療後3年の今、64kg前後で増え気味)。これらの症状は治療後2週間目から徐々に緩和。立ち小便が可能になった。間もなく日常生活も正常に。ふらふらの体でウオーキングを再開。
・ハルナール(排尿促進)、ベタニス(尿意制御)とガスモチン(腸管蠕動促進)を処方された。排尿最困難時にハルナールを1週間だけ服用したが、原則、薬は敬遠(薬嫌い原理主義者である)。治療終了後、処方されたガスモチンに代えてタケダ漢方胃腸薬(大黄甘草湯)を約1カ月。よく効いた。上記合併症に加えてこの期間、動悸、めまい、ふらつきがあり、ハルナールの副作用か、あるいは、放射線合併症(赤血球の減少)によるものなのか。CRP値(炎症と細胞破壊の程度を示す)の大幅上昇(IMRT直後6.45、現在0.04)に示されるように、体の不如意は、自然な生体防御反応であったと理解している。
・ホルモン治療をいつ止めるかについて率直に泌尿器科主治医に相談。定説が無いとしながらも、医師の同意を得て合計27カ月(ネオアジュバント6+コンカレント2+アジュバント19)で一旦、中止した。HbA1c>7.50のため、リュープリンの副作用である脂質代謝異常やインスリン抵抗性を懸念したため。尚、ALPや肝臓諸数値は正常であり、深刻な発汗(ホットフラッシュ)はまったく無かった。27カ月は、ADT-CAB最適期間であったと信じている(注1)。IMRT後3年、ADT-CAB効果消滅後1年5カ月の今、かさかさの頭髪、すべすべ膚と顔の皮脂は完全に原状回復、勃起と体毛(腋・腿・脛)も顕著に回復途上。乳首の発色は消えたが、ほんの少し膨らんだまま。
・晩期障害として直腸出血、血便と血尿はない。但し、この3年間(注2)、力んだ(下腹部に力を入れる、無理に押し出す)ときに数回、便にごく少量の血痕を認めた。今でも毎回、覗き込んで観察している。癖になった。排尿時に尿道に擦れるような(染みるような)感じが今でもときどきある。夜間排尿回数は、再頻値=2、平均値<2.0。治療前より減少した。但し、就寝時と起床時は含まれない。尿腺は明らかに太くなった。医師によれば、ホルモン剤は通常の前立腺肥大症薬よりはるかに強い効果がある由。便は、色、サイズや長さも改善、快便である。薬は何も使っていない。治療前最大の懸念材料であった晩期障害は楽観している。治療前のときどきの切れ痔が治療後ないのは予想外の負の後遺症。
4.PSA推移
IMRT直前(ADT-CAB5カ月後)‐ 0.02 (ホルモン高感受性と理解している)
治療中・治療後2年(ADT-CAB中断時まで)‐ <0.01
治療後2.5年ADT-CAB中断1年から現在まで3カ月毎‐ 0.02、0.04、0.08(2017年4月、ホルモン効果切れか、男性ホルモン復活の兆しか)
5.その他もろもろ
・特段の食事療法はしていない。前立腺がんで赤身脂身の牛豚肉制限(発覚前は肉が多く、魚や野菜が少なかった、若い頃から)。糖尿病対策で糖質制限努力(甘党、HbA1c≦7.00を確実に維持するため)。ミニトマトとブロッコリーだけは例外なく3食とも食卓に上る。便秘対策(便の柔らかさ調整)で牛乳かなり多めのミルクコーヒーを飲む(長期的に牛乳がこの病に良くないことは承知しているが、短期的な直腸対策を優先。勿論、カルシュウム摂取も考慮)。
・降圧剤(カルシュウム拮抗剤アムロジン2.5㎎)と血糖調整薬(メトグルコ250mg)1日1錠服用中。降圧剤は、その日の血圧次第の間欠服用。
...(続きを読む)
-----------------------------------------------------
2017/06/09 に愛知県がんセンターのデータを追記
-----------------------------------------------------
2017年5月14日にひげの父さんはPCRSGの日本語のPDFの紹介の記事を読み、一覧表を提示した記事を投稿しました。今回その論文、または学会発表のデータに基づく項目を追加し、外照射(IMRT,VMAT)と小線源の比較という観点で書いてみます。
追加したのは5年PSA非再発率と高リスク因子数総計(%)の値です。
高リスク因子数総計(%)は高リスクのリスク因子の% を足したものであり、これが100%ならば、複数のリスク因子を持つ患者は0であるということを示し、その値が大きいと複数のリスクをもつ患者の数が多いことを示します。
表は10の病院からなっており、以下のとおりです。
小線源は高リスク前立腺がんで、トリモダリティーを積極的に実施している施設 前立腺がんの小線源療法 日本メジフィジックス株式会社でページが作成されたときに最初に掲載された3つの病院とさらに追記された徳島大学及び掲載はされていないが、日本で最初に小線源治療を行った東京医療センターです。
外照射は治療法比較3よりいずれもでfull text が確認できたもの5つです。
以下病院名は記さず、番号で記載します。
小線源の場合は残念ながら、PSA(20と超える患者数)のデータが5件中、6,7だけであり、T3以上の患者数、GSが8以上の患者数を足してもあまり意味ないので、欄は空白としています。
<strong>高リスク因子数総計(%) </strong>
外照射は149~180、小線源は128と172 です。値がはっきしない場合が多いですが小線源の場合、外照射の一番少ない値149になるのはPSAが20以上の患者の割合が80%ほどになる必要があり、そのようなことはあまり考えられず、外照射より値は低いと思われます。
すなわち、リスク因子を複数もつ患者は少ない。
<strong>PSA非再発率</strong>
PSA非再発率に関して、総じて小線源のほうがいいと思われるますが、T3以上の患者の割合及び複数 リスク因子の数をもつ患者の数が小線源のほうが外照射より少ないということがみてとれます。
すなわち、小線源と外照射のPSA非再発率の差はそう大きいものではないとみてとれます。それは外照射のほうがリスクの高い患者の治療を行っており、結果としてPSA非再発率も低い値となっていると思われるからです。
もちろん、先の投稿でも書きましたように 小線源の6は例外で高リスク因子数総計(%)、T3患者数の割合は外照射の1 と匹敵し、外照射の一番いいPSA非再発率の1 より少し劣るという状況です。
<strong>高リスク可能治療病院について </strong>
...(続きを読む)
2017/06/09 に愛知県がんセンターのデータを追記
-----------------------------------------------------
2017年5月14日にひげの父さんはPCRSGの日本語のPDFの紹介の記事を読み、一覧表を提示した記事を投稿しました。今回その論文、または学会発表のデータに基づく項目を追加し、外照射(IMRT,VMAT)と小線源の比較という観点で書いてみます。
追加したのは5年PSA非再発率と高リスク因子数総計(%)の値です。
高リスク因子数総計(%)は高リスクのリスク因子の% を足したものであり、これが100%ならば、複数のリスク因子を持つ患者は0であるということを示し、その値が大きいと複数のリスクをもつ患者の数が多いことを示します。
表は10の病院からなっており、以下のとおりです。
小線源は高リスク前立腺がんで、トリモダリティーを積極的に実施している施設 前立腺がんの小線源療法 日本メジフィジックス株式会社でページが作成されたときに最初に掲載された3つの病院とさらに追記された徳島大学及び掲載はされていないが、日本で最初に小線源治療を行った東京医療センターです。
外照射は治療法比較3よりいずれもでfull text が確認できたもの5つです。
以下病院名は記さず、番号で記載します。
小線源の場合は残念ながら、PSA(20と超える患者数)のデータが5件中、6,7だけであり、T3以上の患者数、GSが8以上の患者数を足してもあまり意味ないので、欄は空白としています。
<strong>高リスク因子数総計(%) </strong>
外照射は149~180、小線源は128と172 です。値がはっきしない場合が多いですが小線源の場合、外照射の一番少ない値149になるのはPSAが20以上の患者の割合が80%ほどになる必要があり、そのようなことはあまり考えられず、外照射より値は低いと思われます。
すなわち、リスク因子を複数もつ患者は少ない。
<strong>PSA非再発率</strong>
PSA非再発率に関して、総じて小線源のほうがいいと思われるますが、T3以上の患者の割合及び複数 リスク因子の数をもつ患者の数が小線源のほうが外照射より少ないということがみてとれます。
すなわち、小線源と外照射のPSA非再発率の差はそう大きいものではないとみてとれます。それは外照射のほうがリスクの高い患者の治療を行っており、結果としてPSA非再発率も低い値となっていると思われるからです。
もちろん、先の投稿でも書きましたように 小線源の6は例外で高リスク因子数総計(%)、T3患者数の割合は外照射の1 と匹敵し、外照射の一番いいPSA非再発率の1 より少し劣るという状況です。
<strong>高リスク可能治療病院について </strong>
...(続きを読む)
滋賀医科大学の治療成績について
投稿者:SANZOKU 投稿日:2017/03/17(金) 12:06:46 No.56
[返信]
滋賀医科大学の治療成績について
<論文の概要>
この論文は滋賀医科大学の岡本、河野先生のグループで治療された2005年から2013年までの高リスク患者143名の治療成績についてまとめられたものです。2005年は先生が治療を開始された時期にあたります。5年非再発率が95.2%と高リスク患者を対象とした結果では他にない好成績です。高リスクと言ってもリスク要因が1つの患者が60名(42%)、2つが61名(43%)、3つが22名(15%)と並外れた高リスクであり(詳細はTable1&2)、しかも前立腺近傍のリンパ節転移1~2個を有する患者5名を含んでいます。
この内不幸にして再発された患者さんは6名になります。この6名の方は全員、外部照射終了から12―30ヶ月でPSA再発をきたし、その後0―18ヶ月で骨転移を確認しています。つまり全員5年以内に骨転移による臨床再発をきたした訳です。特筆すべきは、リンパ節転移を有した患者さんが再発していないことです。そして前立腺癌による死亡が1名あり、他の原因で死亡した患者さんが3名いました。
それではこのような好成績を収めた治療法について説明します。先ず、全ての患者さんがホルモン治療、小線源、外部照射を併用するトリモダリティを受けています。ホルモン治療はLH-RHアゴニストと抗男性ホルモン剤を併用するMAB療法です。そして原則として小線源前6ヶ月のネオアジュバントと、その後は6ヶ月のアジュバントを行っています。小線源治療は経直腸超音波エコーを用い、125I線源をリアルタイム術中計画法で前立腺に留置します。また癌の位置によっては精嚢にも留置します。処方線量は通常D90にて135~145Gy程度になります。D90とは前立腺体積の90%に照射される最低線量で、これはBED(生物学的実効線量)に換算すると141~153Gyになります。小線源と合わせた総線量をBEDで220Gy以上確保するため、小線源施術1ヶ月後のポストプランで外部照射の処方を決めます。外部照射は3次元原体照射にて行います。その線量は1回1.8Gy、総線量は45Gyを中央値としています。そして前立腺と精嚢辺縁に15mmのマージンをとって照射します。ただし他臓器近辺は7~10mmにします。リンパ節転移を有する患者ならびに非常にリスクの高い患者は、それ以外にも骨盤内全般の照射も行います。これら全ての照射はUD30ならびにR100を担保します。
実際に患者さんに施された線量はTable3、Table4にまとめられています。
*UD30(Gy) : 尿道線量の指標で尿道体積の30%が受ける線量
小線源単独療法:200Gy未満 (術後210Gyを超えないように)
外部照射併用療法:160Gy未満 (術後165Gyを超えないように)
*Rectal V100(cc):直腸線量の指標で処方線量の100%以上が照射され
ている直腸体積
小線源単独療法:0.5cc未満
外部照射併用療法:0.2cc未満
いくら好成績であったとしても、有害事象が多ければ元も子もありません。論文ではグレード2の急性障害が直腸に1.3%、泌尿生殖器に10.4%あったそうです。またグレード2の晩期障害はそれぞれ2.0%と4.1%です。それ以上のグレードの有害事象はありません。治療としては末期の腎臓障害による血球減少にともなうグレード2の直腸出血をきたした患者1名が高圧酸素療法を受けました。また直腸出血はなかったが、特発性血小板欠乏症の患者1名が血小板輸血を受けました。尿道狭窄、経尿道切除術、直腸尿道瘻はありませんでした。
*有害事象のグレード
Grade 1 軽症 症状がないまたは軽度の症状がある。臨床所見または検査所見のみ。治療を要さない。
Grade 2中等症 最小限局所的非侵襲的治療を要する。年齢相応の身の回り以外の日常生活動作の制限。
Grade 3 重症または医学的に重大であるが、ただちに生命を脅かすものではない。
入院または入院期間の延長を要する。活動不能、動作不能。身の回りの日常生活動作の制限。
Grade 4 生命を脅かす 緊急処置を要する。
Grade 5 有害事象による死亡
その他私が気になったところを補足します。まずFig1と2の説明です。Fig1はA.PSA非再発率、B.臨床非再発率、C.前立腺癌生存率、D.全生存率です。勘の鋭い方は、PSA非再発率>臨床非再発率の関係に疑問を抱かれると思います。これはPSA再発率<臨床再発率を意味しているからです。論文を読めば分かることですが、実際はPSA再発率=臨床再発率なのですが、統計処理に用いられているカプランマイヤー法ではこのような奇妙な結果になるのです。簡単に説明すると、カプランマイヤー法では年数を経るにつれて、母数が減少するので1イベントの重みが大きくなるのです。臨床再発はPSA再発の後に生じるので、1イベントの比重が大きくなる訳です。あくまで統計処理なので、このような曖昧さが介在することに注意しなければなりません。
次にFig2は、精嚢浸潤とリンパ節転移を有する患者さんの患部の画像とその患者の治療後のPSA経過です。画像は専門家でないとよく分かりませんが、治療後の経過は極めて順調ですね。
論文で特に興味を持った点は、必ずしも転移がリスク要因の数と関係していない点です。再発患者6名の内、4名が1リスク(4/60=6.7%)、1名が2リスク(1/61=1.6%)、1名が3リスク(1/22=4.5%)です。患者数が少ないのでこれだけで結論できませんが興味深い結果です。転移はリスク要因とは別の要素を原因としているかもしれないと暗示しているからです。
私の解説ですので、間違いや勘違い独断があると思います。これを読んでご興味を持たれた方は是非とも原論文を読んで確かめてください。
https://www.termedia.pl/High-biologically-effective-dose-radiation-therapy-using-brachytherapy-in-combination-with-external-beam-radiotherapy-for-high-risk-prostate-cancer,54,29511,1,1.html
...(続きを読む)
<論文の概要>
この論文は滋賀医科大学の岡本、河野先生のグループで治療された2005年から2013年までの高リスク患者143名の治療成績についてまとめられたものです。2005年は先生が治療を開始された時期にあたります。5年非再発率が95.2%と高リスク患者を対象とした結果では他にない好成績です。高リスクと言ってもリスク要因が1つの患者が60名(42%)、2つが61名(43%)、3つが22名(15%)と並外れた高リスクであり(詳細はTable1&2)、しかも前立腺近傍のリンパ節転移1~2個を有する患者5名を含んでいます。
この内不幸にして再発された患者さんは6名になります。この6名の方は全員、外部照射終了から12―30ヶ月でPSA再発をきたし、その後0―18ヶ月で骨転移を確認しています。つまり全員5年以内に骨転移による臨床再発をきたした訳です。特筆すべきは、リンパ節転移を有した患者さんが再発していないことです。そして前立腺癌による死亡が1名あり、他の原因で死亡した患者さんが3名いました。
それではこのような好成績を収めた治療法について説明します。先ず、全ての患者さんがホルモン治療、小線源、外部照射を併用するトリモダリティを受けています。ホルモン治療はLH-RHアゴニストと抗男性ホルモン剤を併用するMAB療法です。そして原則として小線源前6ヶ月のネオアジュバントと、その後は6ヶ月のアジュバントを行っています。小線源治療は経直腸超音波エコーを用い、125I線源をリアルタイム術中計画法で前立腺に留置します。また癌の位置によっては精嚢にも留置します。処方線量は通常D90にて135~145Gy程度になります。D90とは前立腺体積の90%に照射される最低線量で、これはBED(生物学的実効線量)に換算すると141~153Gyになります。小線源と合わせた総線量をBEDで220Gy以上確保するため、小線源施術1ヶ月後のポストプランで外部照射の処方を決めます。外部照射は3次元原体照射にて行います。その線量は1回1.8Gy、総線量は45Gyを中央値としています。そして前立腺と精嚢辺縁に15mmのマージンをとって照射します。ただし他臓器近辺は7~10mmにします。リンパ節転移を有する患者ならびに非常にリスクの高い患者は、それ以外にも骨盤内全般の照射も行います。これら全ての照射はUD30ならびにR100を担保します。
実際に患者さんに施された線量はTable3、Table4にまとめられています。
*UD30(Gy) : 尿道線量の指標で尿道体積の30%が受ける線量
小線源単独療法:200Gy未満 (術後210Gyを超えないように)
外部照射併用療法:160Gy未満 (術後165Gyを超えないように)
*Rectal V100(cc):直腸線量の指標で処方線量の100%以上が照射され
ている直腸体積
小線源単独療法:0.5cc未満
外部照射併用療法:0.2cc未満
いくら好成績であったとしても、有害事象が多ければ元も子もありません。論文ではグレード2の急性障害が直腸に1.3%、泌尿生殖器に10.4%あったそうです。またグレード2の晩期障害はそれぞれ2.0%と4.1%です。それ以上のグレードの有害事象はありません。治療としては末期の腎臓障害による血球減少にともなうグレード2の直腸出血をきたした患者1名が高圧酸素療法を受けました。また直腸出血はなかったが、特発性血小板欠乏症の患者1名が血小板輸血を受けました。尿道狭窄、経尿道切除術、直腸尿道瘻はありませんでした。
*有害事象のグレード
Grade 1 軽症 症状がないまたは軽度の症状がある。臨床所見または検査所見のみ。治療を要さない。
Grade 2中等症 最小限局所的非侵襲的治療を要する。年齢相応の身の回り以外の日常生活動作の制限。
Grade 3 重症または医学的に重大であるが、ただちに生命を脅かすものではない。
入院または入院期間の延長を要する。活動不能、動作不能。身の回りの日常生活動作の制限。
Grade 4 生命を脅かす 緊急処置を要する。
Grade 5 有害事象による死亡
その他私が気になったところを補足します。まずFig1と2の説明です。Fig1はA.PSA非再発率、B.臨床非再発率、C.前立腺癌生存率、D.全生存率です。勘の鋭い方は、PSA非再発率>臨床非再発率の関係に疑問を抱かれると思います。これはPSA再発率<臨床再発率を意味しているからです。論文を読めば分かることですが、実際はPSA再発率=臨床再発率なのですが、統計処理に用いられているカプランマイヤー法ではこのような奇妙な結果になるのです。簡単に説明すると、カプランマイヤー法では年数を経るにつれて、母数が減少するので1イベントの重みが大きくなるのです。臨床再発はPSA再発の後に生じるので、1イベントの比重が大きくなる訳です。あくまで統計処理なので、このような曖昧さが介在することに注意しなければなりません。
次にFig2は、精嚢浸潤とリンパ節転移を有する患者さんの患部の画像とその患者の治療後のPSA経過です。画像は専門家でないとよく分かりませんが、治療後の経過は極めて順調ですね。
論文で特に興味を持った点は、必ずしも転移がリスク要因の数と関係していない点です。再発患者6名の内、4名が1リスク(4/60=6.7%)、1名が2リスク(1/61=1.6%)、1名が3リスク(1/22=4.5%)です。患者数が少ないのでこれだけで結論できませんが興味深い結果です。転移はリスク要因とは別の要素を原因としているかもしれないと暗示しているからです。
私の解説ですので、間違いや勘違い独断があると思います。これを読んでご興味を持たれた方は是非とも原論文を読んで確かめてください。
https://www.termedia.pl/High-biologically-effective-dose-radiation-therapy-using-brachytherapy-in-combination-with-external-beam-radiotherapy-for-high-risk-prostate-cancer,54,29511,1,1.html
...(続きを読む)
滋賀医大 岡本らの論文
投稿者:漂流 投稿日:2017/03/15(水) 00:50:40 No.54
[返信]
http://www.termedia.pl/High-biologically-effective-dose-radiation-therapy-using-brachytherapy-in-combination-with-external-beam-radiotherapy-for-high-risk-prostate-cancer,54,29511,1,1.html
High biologically effective dose radiation therapy using brachytherapy in combination with external beam radiotherapy for high-risk prostate cancer
Keisei Okamoto, MD, PhD1, Akinori Wada, MD2, Naoaki Kohno, MD, PhD3
1Department of Brachytherapy for Prostate Cancer, 2Department of Urology, 3Department of Radiology, Shiga University of Medical Science,
Shiga, Japan
タイトル
内部照射と外部照射との組み合わせによる、高BED(biologically effective dose: 生物学的等価線量)での高リスク前立腺癌の治療
目的: 低線量率内部照射(LDR)、外部照射(EBRT)、そして、短期間アンドロゲン遮断療法(ADT)を組み合わせて、220Gyを超えるBEDで、高リスク前立腺癌を治療し、その成果を評価すること。
材料と方法: 2005年から2013年のまでの間、高リスク前立腺癌を患った143人に対して、LDR, EBRT, そして短期ADTを組み合わせてBED ? 220 Gyの放射線治療を施した。本研究での「高リスク前立腺癌の患者」は、高リスクと超高リスク前立腺癌患者から構成されていた。具体的には、60人は高リスク因子を一つ(42%)、61人は高リスク因子を二つ(43%)、そして、残りの22人は高リスク因子を三つ(15%)、このうち5人はリンパ節転移が認められた。 EBRTは癌の広がり方を勘案して、前立腺と精嚢だけに照射するか或いは、全骨盤照射を行った。
結果: 6人の患者は生化学的再発(PSAの再燃)が明らかとなったので、5年の実質生化学的非再発率は95.2%となった。生化学的再発は、本研究では、遠隔転移の症例でもあった。この生化学的再発をした6人は、骨転移という臨床的再発に至った。このことから、5年臨床的非再発率は、計算上、93.0%となった。リンパ節転移の患者については、何方も、生化学的再発は認められなかった。本研究の追跡で、前立腺癌が原因で亡くなられた1人を含め、計4人の方が亡くなられた。従って疾病特異的生存率は、97.2%、そして、全生存率は、95.5%と計算された。
結論: LDRとEBRT を組み合わせて、BED ? 220 Gy照射は、生化学的非再発率において、卓越した成績をもたらすことが示された。
ここでは、スペースの関係で、抄録しか翻訳していませんが、この抄録からも判りますが、全文を読むと以下の事が明確に判ります。
生化学的再発は6人に認められ、ADT終了後、中央値23(12-30)ヶ月であること、遠隔転移は、その後、中央値9(0-18)ヶ月で確認された。このような短期間でのPSA再燃、そして、遠隔転移は、治療開始前に、既に、遠隔転移していたことを示しています。それを裏付ける証拠として、生化学的再発した6人は、前立腺内での癌の再発は認められなかったのです。
治療の段階で、既に遠隔転移している前立腺癌については、征圧出来ませんでしたが、前立腺内にある癌細胞、更には、骨盤内のリンパ節に転移している癌細胞は、完全に征圧することが出来ています。 つまり、遠隔転移がなければ、岡本らのこの治療法で、限局性前立腺癌、そして、たとえ、リンパ節転移があっても骨盤内であれば、完全に征圧(やっつける)ことが出来ることを示しています。
High biologically effective dose radiation therapy using brachytherapy in combination with external beam radiotherapy for high-risk prostate cancer
Keisei Okamoto, MD, PhD1, Akinori Wada, MD2, Naoaki Kohno, MD, PhD3
1Department of Brachytherapy for Prostate Cancer, 2Department of Urology, 3Department of Radiology, Shiga University of Medical Science,
Shiga, Japan
タイトル
内部照射と外部照射との組み合わせによる、高BED(biologically effective dose: 生物学的等価線量)での高リスク前立腺癌の治療
目的: 低線量率内部照射(LDR)、外部照射(EBRT)、そして、短期間アンドロゲン遮断療法(ADT)を組み合わせて、220Gyを超えるBEDで、高リスク前立腺癌を治療し、その成果を評価すること。
材料と方法: 2005年から2013年のまでの間、高リスク前立腺癌を患った143人に対して、LDR, EBRT, そして短期ADTを組み合わせてBED ? 220 Gyの放射線治療を施した。本研究での「高リスク前立腺癌の患者」は、高リスクと超高リスク前立腺癌患者から構成されていた。具体的には、60人は高リスク因子を一つ(42%)、61人は高リスク因子を二つ(43%)、そして、残りの22人は高リスク因子を三つ(15%)、このうち5人はリンパ節転移が認められた。 EBRTは癌の広がり方を勘案して、前立腺と精嚢だけに照射するか或いは、全骨盤照射を行った。
結果: 6人の患者は生化学的再発(PSAの再燃)が明らかとなったので、5年の実質生化学的非再発率は95.2%となった。生化学的再発は、本研究では、遠隔転移の症例でもあった。この生化学的再発をした6人は、骨転移という臨床的再発に至った。このことから、5年臨床的非再発率は、計算上、93.0%となった。リンパ節転移の患者については、何方も、生化学的再発は認められなかった。本研究の追跡で、前立腺癌が原因で亡くなられた1人を含め、計4人の方が亡くなられた。従って疾病特異的生存率は、97.2%、そして、全生存率は、95.5%と計算された。
結論: LDRとEBRT を組み合わせて、BED ? 220 Gy照射は、生化学的非再発率において、卓越した成績をもたらすことが示された。
ここでは、スペースの関係で、抄録しか翻訳していませんが、この抄録からも判りますが、全文を読むと以下の事が明確に判ります。
生化学的再発は6人に認められ、ADT終了後、中央値23(12-30)ヶ月であること、遠隔転移は、その後、中央値9(0-18)ヶ月で確認された。このような短期間でのPSA再燃、そして、遠隔転移は、治療開始前に、既に、遠隔転移していたことを示しています。それを裏付ける証拠として、生化学的再発した6人は、前立腺内での癌の再発は認められなかったのです。
治療の段階で、既に遠隔転移している前立腺癌については、征圧出来ませんでしたが、前立腺内にある癌細胞、更には、骨盤内のリンパ節に転移している癌細胞は、完全に征圧することが出来ています。 つまり、遠隔転移がなければ、岡本らのこの治療法で、限局性前立腺癌、そして、たとえ、リンパ節転移があっても骨盤内であれば、完全に征圧(やっつける)ことが出来ることを示しています。
滋賀医大岡本氏らの論文;抄録
投稿者:ひげの父さん 投稿日:2017/03/15(水) 01:28:32 No.55
すでに漂流さんが訳されていますが、直訳気味で少し分かりにくいと思うので(失礼)、私の別訳も紹介しておきます。
目的:
高リスク前立腺癌に対する、低線量率ブラキセラピー(LDR)と外部照射(EBRT)および短期ホルモン療法(ADT)の組合せによる高線量放射線療法(生物学的等価線量:BED 220Gy以上)の成績を評価する。
対象と治療法:
2005年から2013年にかけて、高リスクおよび超高リスク前立腺癌患者143名が、LDR+EBRT+ADTの併用によるBED≧220 Gyの放射線量による治療を受けた。
高リスクの因子数は、1つだけが60例(42%)、2つが61例(43%)、3つとも高リスクであったのが22例(15%)であり、これには5人のリンパ節転移を有する疾患も含まれている。
外部照射の範囲は、疾患の広がりに応じて、前立腺および精嚢のみの場合と全骨盤域を含む場合がある。
生化学的再発はフェニックスの定義による。
結果:
6人が生化学的再発を発症し、5年生化学的非再発生存率(BFFS)95.2%が得られたが、生化学的再発(遠隔転移)を認められた6人の患者は、全て骨転移による臨床的再発を有しているため、5年臨床的非再発率(FFCF)は93.0%となる。
リンパ節転移のある症例については、いずれも生化学的再発には到らなかった。
死亡4名には前立腺癌特異的死亡も含まれており、疾患特異的生存率(CSS)は97.2%、全生存率(OS)は95.5%であった。
結論:
生物学的等価線量(BED)と生化学的非再発生存率(BFFS)との関係立証にはさらなる検証が必要だが、低線量率ブラキセラピー(LDR)と外部照射(EBRT)の併用による高線量(BED≧220Gy)放射線療法は、高リスクおよび超高リスク前立腺がんを対象とする5年生化学的非再発生存率(BFFS)において、優れた結果を示すことができた。
目的:
高リスク前立腺癌に対する、低線量率ブラキセラピー(LDR)と外部照射(EBRT)および短期ホルモン療法(ADT)の組合せによる高線量放射線療法(生物学的等価線量:BED 220Gy以上)の成績を評価する。
対象と治療法:
2005年から2013年にかけて、高リスクおよび超高リスク前立腺癌患者143名が、LDR+EBRT+ADTの併用によるBED≧220 Gyの放射線量による治療を受けた。
高リスクの因子数は、1つだけが60例(42%)、2つが61例(43%)、3つとも高リスクであったのが22例(15%)であり、これには5人のリンパ節転移を有する疾患も含まれている。
外部照射の範囲は、疾患の広がりに応じて、前立腺および精嚢のみの場合と全骨盤域を含む場合がある。
生化学的再発はフェニックスの定義による。
結果:
6人が生化学的再発を発症し、5年生化学的非再発生存率(BFFS)95.2%が得られたが、生化学的再発(遠隔転移)を認められた6人の患者は、全て骨転移による臨床的再発を有しているため、5年臨床的非再発率(FFCF)は93.0%となる。
リンパ節転移のある症例については、いずれも生化学的再発には到らなかった。
死亡4名には前立腺癌特異的死亡も含まれており、疾患特異的生存率(CSS)は97.2%、全生存率(OS)は95.5%であった。
結論:
生物学的等価線量(BED)と生化学的非再発生存率(BFFS)との関係立証にはさらなる検証が必要だが、低線量率ブラキセラピー(LDR)と外部照射(EBRT)の併用による高線量(BED≧220Gy)放射線療法は、高リスクおよび超高リスク前立腺がんを対象とする5年生化学的非再発生存率(BFFS)において、優れた結果を示すことができた。
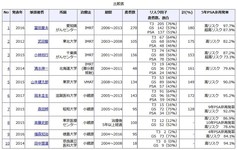
治療法別PSA非再発率の比較表 (改訂)で今まで調べた論文に掲載されているPSA非再発率の比較表を示しました。
今回、その後に調べたものを含め計39の論文の一覧を示します。
なおサイトには治療法比較3と題して、原論文へのリンク、サイトへのリンクの一覧表のページを公開しています。
表はオーストラリアでIMRTによる治療を実施し、オーストラリアの他の治療法との比較を実施した Shea William Wilcox 氏の論文、J Med Imaging Radiat Oncol. 2015 Feb;59(1):125-33に載せられている表を参考にしたものです。
リスク分類に関しては、患者の内訳(%)及び、NCCNリスク分類かD'Amicoリスク分類を示しました。
PCRTFのデータべースに受け入れる条件、Acceptance Criteriaには以下のように書かれています。
Only peer reviewed journals are included. Peer reviewed journals
are those in which every article is first reviewed by an expert panel
before publication.
ここで一覧表にあげた論文はピア・レビュー(査読)付きジャーナルに載ったものばかりということではないです。
博士論文、学会発表が学会誌に載ったもの等が含まれています。また、追跡期間なども特に規定していません。サイトを立ち上げ、営々と論文紹介をしたもののまとめです。
なお、ホルモン治療に関する情報は特に記載していません。
今回、その後に調べたものを含め計39の論文の一覧を示します。
なおサイトには治療法比較3と題して、原論文へのリンク、サイトへのリンクの一覧表のページを公開しています。
表はオーストラリアでIMRTによる治療を実施し、オーストラリアの他の治療法との比較を実施した Shea William Wilcox 氏の論文、J Med Imaging Radiat Oncol. 2015 Feb;59(1):125-33に載せられている表を参考にしたものです。
リスク分類に関しては、患者の内訳(%)及び、NCCNリスク分類かD'Amicoリスク分類を示しました。
PCRTFのデータべースに受け入れる条件、Acceptance Criteriaには以下のように書かれています。
Only peer reviewed journals are included. Peer reviewed journals
are those in which every article is first reviewed by an expert panel
before publication.
ここで一覧表にあげた論文はピア・レビュー(査読)付きジャーナルに載ったものばかりということではないです。
博士論文、学会発表が学会誌に載ったもの等が含まれています。また、追跡期間なども特に規定していません。サイトを立ち上げ、営々と論文紹介をしたもののまとめです。
なお、ホルモン治療に関する情報は特に記載していません。
ブログでVMATという記事を書き、東大、筑波大の博士論文でVMATを使用した治療成績を記述した東京大学 山本健太郎氏の論文の概要を紹介しました。その論文は以下の表題です。
・ コーンビームCTによる画像誘導放射線治療を併用した前立腺癌に対する強度変調回転照射の検討
論文は日本語で書かれているので、特に説明することはそうないかと思いますが、印象に残ったことをもう少し詳しくみて、以下に記述します。
治療装置に関しては、次のように書かれています。
東京大学医学部附属病院(以下当院と略す)では2007年にElekta社のSynergy
という治療装置を世界で先駆けて導入し、臨床研究を開始した[24]。
さらに前立腺の移動に関しては論文[27]の図を参照し、以下のように書かれています。
毎回の治療時の前立腺の移動量は、左右方向では2mm、前後・頭尾側方向では概ね
4mm以内に収まっていることが確認できた。
動く前立腺で前立腺の移動に関して調べたことを書きました。この論文では以下のように書かれています。
Shimizuらは、前立腺内に埋め込まれた金マーカーの治療時の移動を透視画像で
解析し、治療開始後2分以内であれば前立腺の移動量は前後、左右、上下ともに
2mm以内に収まっていたが、それ以上経過すると大きく変位することを報告して
いる[29]。
論文は2008年8月から2013年3月までにVMATで治療し、1年以上経過観察を実施した一連の前立腺がん患者287名が対象です。1回線量2 Gyで週5回、計38回 76 Gy での治療です。
患者の状況は以下のとおり。
年齢中央値71 (範囲, 48-84)
...(続きを読む)
・ コーンビームCTによる画像誘導放射線治療を併用した前立腺癌に対する強度変調回転照射の検討
論文は日本語で書かれているので、特に説明することはそうないかと思いますが、印象に残ったことをもう少し詳しくみて、以下に記述します。
治療装置に関しては、次のように書かれています。
東京大学医学部附属病院(以下当院と略す)では2007年にElekta社のSynergy
という治療装置を世界で先駆けて導入し、臨床研究を開始した[24]。
さらに前立腺の移動に関しては論文[27]の図を参照し、以下のように書かれています。
毎回の治療時の前立腺の移動量は、左右方向では2mm、前後・頭尾側方向では概ね
4mm以内に収まっていることが確認できた。
動く前立腺で前立腺の移動に関して調べたことを書きました。この論文では以下のように書かれています。
Shimizuらは、前立腺内に埋め込まれた金マーカーの治療時の移動を透視画像で
解析し、治療開始後2分以内であれば前立腺の移動量は前後、左右、上下ともに
2mm以内に収まっていたが、それ以上経過すると大きく変位することを報告して
いる[29]。
論文は2008年8月から2013年3月までにVMATで治療し、1年以上経過観察を実施した一連の前立腺がん患者287名が対象です。1回線量2 Gyで週5回、計38回 76 Gy での治療です。
患者の状況は以下のとおり。
年齢中央値71 (範囲, 48-84)
...(続きを読む)